题目内容
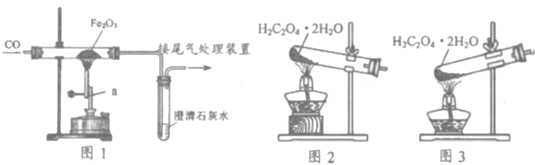
【题目】固体混合物A是由Mg、CuO、Na2SO4、Na2CO3、BaCl2、BaSO4中的几种混合而成,为确定其成分,进行如图实验.(假设每步反应均恰好完全反应)下面推断不正确的是
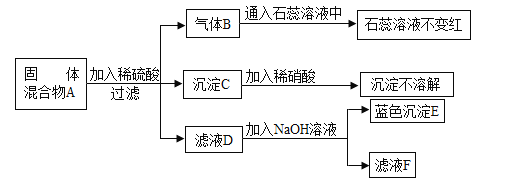
A. 由气体B可推原固体混合物A中一定含有Mg,一定不含Na2CO3
B. 沉淀C一定为BaSO4,由此可推原固体混合物A中一定含有BaCl2和Na2SO4
C. 滤液D中一定含有的溶质是MgSO4和CuSO4
D. 固体A的组成可能有6种
【答案】B
【解析】
A. Mg、CuO、Na2SO4、Na2CO3、BaCl2、BaSO4中只有碳酸钠和镁都能与酸反应生成气体,其中镁与酸反应生成氢气,碳酸钠与酸反应生成二氧化碳,二氧化碳和水反应生成碳酸,能使紫色石蕊试液变红,而实验气体B不能使紫色石蕊试液变红,可推原固体混合物A中一定含有Mg,一定不含Na2CO3,选项正确;
B.硫酸钡沉淀不溶于硝酸,沉淀C一定为BaSO4,但硫酸钡可能是硫酸和氯化钡反应生成,也可能是硫酸钠与氯化钡反应生成,还可能是原固体中有硫酸钡,由此不可推原固体混合物是否有BaCl2、 Na2SO4,选项错误;
C.硫酸铜和氢氧化钠反应生成蓝色氢氧化铜沉淀,滤液D中一定含有的溶质是CuSO4,原固体中一定有氧化铜,硫酸和镁反应生成硫酸镁,滤液D中一定有MgSO4,选项正确;
D. 固体A的组成可能有①氧化铜、镁、硫酸钡,②氧化铜、镁、氯化钡,③氧化铜、镁、硫酸钡、硫酸钠,④氧化铜、镁、氯化钡、硫酸钠,⑤氧化铜、镁、硫酸钡、氯化钡,⑥氧化铜、镁、硫酸钡、氯化钡、硫酸钠,共6种,故D正确。
故选C。

【题目】某小组同学为探究二氧化锰对过氧化氢分解速度的影响,设计了以下实验:
(1)完善实验一、实验二:
实验步骤 | 实验现象 | 实验结论 | |
实验一 |
| 带火星的木条不复燃 | 过氧化氢分解的速率较慢 |
实验二 |
| ___________ | ________ |
(2)实验三:待实验二结束,剩余的液体化学式为_____,倒出多余液体,继续向其中加入5%的过氧化氢溶液,实验现象为____________,得出结论__________,写出此时的反应方程式__________;
(3)实验四,实验之前称量加入二氧化锰的质量为m1,待实验三结束后,取出二氧化锰,干燥后称量质量为m2,则m1_____m2(填“>”、“<”、“=”),得出结论___________,从液体中取出二氧化锰的操作名称为______;