题目内容
【题目】某山区盛产石灰石,其中含有的杂质为二氧化硅(不溶于水、高温下难以分解的酸性氧化物).S中学初三化学研究性学习小组的同学为了测定某矿山石灰石的纯度,取2.0g该矿山石灰石样品,将20.0g盐酸平均分成4份,分4次入到样品中,充分反应后测定剩余固体的质量,数据见表.试求:
次数 | 1 | 2 | 3 | 4 |
加入盐酸质量/g | 5.0 | 5.0 | 5.0 | 5.0 |
剩余固体质量/g | 1.3 | 0.6 | 0.2 | 0.2 |
(1)2.0g石灰石样品中杂质的质量.
(2)石灰石样品中碳酸钙的质量分数.
(3)加入的盐酸中溶质的质量分数是多少?
【答案】0.2g 90% 10.22﹪
【解析】
固体减少的质量是参加反应的碳酸钙的质量,加入盐酸后固体质量不再减少,说明不再减少的固体是杂质。
(1)根据第一次和第二次加入盐酸后,固体质量都减少0.7g可知,5g的盐酸能反应掉0.7g的碳酸钙,而第三次加入0.5g盐酸后,固体质量减少0.6g-0.2g=0.4g,说明0.2g是杂质。
(2)石灰石样品中碳酸钙的质量为:2.0g-0.2g=1.8g
石灰石样品中碳酸钙的质量分数为:![]() ×100%=90%
×100%=90%
(3)设加入的盐酸中溶质的质量分数是x。
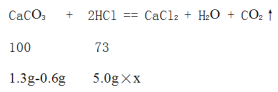
![]() =
=![]()
解得x=10.22﹪

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
【题目】甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
物质 | 甲烷 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 3.2 | 11.2 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
下列判断正确的是
A.表中a的值为2.6 B.X一定是该反应的催化剂
C.X可能含有氢元素 D.X一定含有氧元素