题目内容
【题目】写出下列符号中“2”表示的意义:
(1)Fe2+_____;
(2)![]() _____;
_____;
(3)2CO2_____,_____。
【答案】一个亚铁离子带两个单位的正电荷 铁元素的化合价是+2价 前面的2表示两个二氧化碳分子 后面的2表示一个二氧化碳分子中含有两个氧原子
【解析】
(1)右上角的数字表示一个离子所带的电荷数,Fe2+表示一个亚铁离子带两个单位的正电荷;故表示一个亚铁离子带两个单位的正电荷。
(2)元素正上方的数字表示元素的化合价,![]() 表示铁元素的化合价是+2价,故表示铁元素的化合价是+2价。
表示铁元素的化合价是+2价,故表示铁元素的化合价是+2价。
(3)符号前面的数字,表示原子、分子或离子的个数;2CO2前面的2表示两个二氧化碳分子,后面的2表示一个二氧化碳分子中含有两个氧原子;故表示前面的2表示两个二氧化碳分子;后面的2表示一个二氧化碳分子中含有两个氧原子。

【题目】请完成下列实验,回答问题。
(1)某同学将氢气与空气混合,在安全保障下在老师指导下点燃,实验如下
V(H2)/V(空气) | 1:99 | 3:97 | 4:96 | 50:50 | 70:30 | 75:25 |
点火 | 不炸 | 不炸 | 炸 | 炸 | 炸 | 不炸 |
①该实验说明氢气的爆炸极限范围可能为______~______之间(用百分数表示)
②鉴于该实验爆炸的危险性,说明点燃氢气前必须验纯,验纯的操作为_____
③该实验证明水是由__________________组成的。
(2)除去下列物质中的杂质,所用试剂错误的是___
选项 | 物质 | 杂质 | 除杂试剂 |
A | 铜 | 氧化铜 | 稀硫酸 |
B | 二氧化碳 | 水蒸气 | 生石灰 |
C | 盐酸 | 硫酸 | 氯化钡溶液 |
D | 氯化钡溶 | 氯化钠溶液 | 碳酸钠溶液 |
【题目】分类,类比是初中化学常用的学习方法。
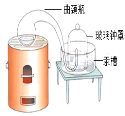
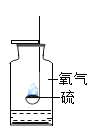
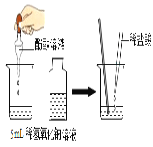
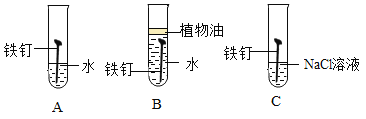
(1)初中化学有许多实验,若按照实验方法分类,可将实验_____(填字母)分为一类;分类的依是_____。
|
|
|
|
A.测定空气中氧气的含量 | B.探究硫在氧气中燃烧 | C.探究反应前后物质的质量关系 | D.探究酸和碱能否发生反应 |
(2)磷酸盐,磷酸氢盐的溶解性和碳酸盐相似,磷酸二氢盐和碳酸氢盐溶解性相似,则磷酸钡的溶解性为_____(填“可溶”或“微溶”或“难溶”),碳酸钙可以和水、二氧化碳(看做碳酸)反应生成碳酸氢钙,请写出向磷酸钙固体中加入磷酸(H3PO4)溶液后,固体消失的反应的化学方程式_____。