题目内容
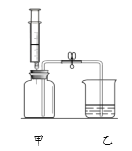
【题目】在一定量AgNO3和Al(NO3)3的混合液中加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则:

①固体乙中一定含有Ag,可能含有Cu和Zn
②溶液甲中一定含有Al(NO3)3和Zn(NO3)2
③若溶液甲是蓝色,则溶液甲中一定有Al(NO3)3、Cu(NO3)2和Zn(NO3)2
④若溶液甲是无色,则溶液甲中一定有Al(NO3)3、可能有Zn(NO3)2、一定没有Cu(NO3)2
⑤向固体乙滴加盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2
上述四种说法正确的个数为 ( )
A. 1个 B. 2个 C. 3个 D. 4个
【答案】D
【解析】金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au,在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的活动性越强。位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。在一定量AgNO3和Al(NO3)3的混合液中加入铜粉和锌粉,锌先与硝酸银反应生成硝酸锌和银,然后铜与硝酸银溶液反应生成硝酸铜和银,但都不与硝酸铝反应,即溶液中一定有硝酸铝、硝酸锌,固体中一定有银。①当锌粉较多,只有锌与硝酸银发生反应且有剩余时,固体乙中一定含有Ag、Cu和Zn,当锌的量较少时,一定有银,铜和锌不确定,①正确;②由于锌一定能反应,故溶液甲中一定含有Al(NO3)3和Zn(NO3)2,正确;③若溶液甲是蓝色,说明溶液中有硝酸铜,则溶液甲中一定有Al(NO3)3、Cu(NO3)2和Zn(NO3)2,正确;④若溶液甲是无色,则溶液甲中一定有Al(NO3)3、Zn(NO3)2,一定没有Cu(NO3)2,错误;⑤向固体乙滴加盐酸有气泡产生,说明锌有剩余,硝酸银一定被反应完,则溶液甲中一定没有AgNO3,铜没有参与反应,溶液中一定没有Cu(NO3)2;故选D。

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
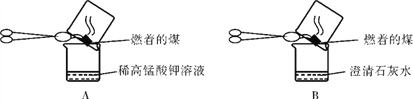
名师指导一卷通系列答案【题目】(1)人类使用的化石燃料主要是煤、石油和________________,直接燃煤会形成严重的酸雨,酸雨是指pH小于______________的降水;
(2)为减少温室气体二氧化碳的排放,可以将二氧化碳进行转化。下图为该反应的微观示意图,根据图示回答下列问题:
反应前 | 反应后 |
| ||
A | B | C | D | |
|
|
|
| |
①以上4种物质中属于有机化合物的是________________(填化学式);
②在反应中C与D质量比为____________________;
(3)氢能是理想的清洁能源。以太阳能为热源,经由铁氧化合物循环分解水的过程如图:
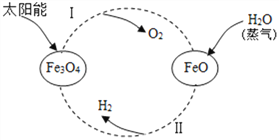
①反应Ⅰ的基本反应类型为___________________;
②写出在一定条件下发生的反应的Ⅱ化学方程式:_____________;
③在上述循环过程中,最终得到的产品是________。
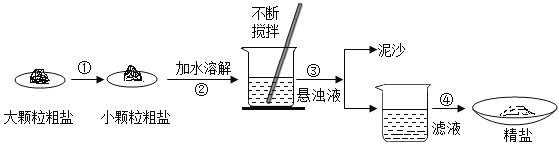
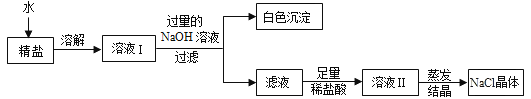
【题目】“低钠盐”可以控制钠的摄入量从而防治高血压等疾病。制备“低钠盐”是在食盐中用NaCl按照配方比例添加食用KCl。国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2)。
(1)测得某“低钠盐”样品a中只含有NaCl和KCl,该样品中的NaCl和KCl溶于
水时解离出的阴离子都是___________(填离子符号)。
(2)探究某“低钠盐”样品b中是否添加有镁盐,以及添加的是何种镁盐?
【猜想】I、不含镁盐 Ⅱ、含有硫酸镁 Ⅲ、含有氯化镁

【进行实验】
(3)请完成下表(已知BaSO4是难溶于水和酸的白色固体):
假设和现象 | 判断和化学方程式 | |
① | 若现象a为白色沉淀 | 则猜想____不成立。 |
② | 若现象a为_________, 现象b为_________。 | 则猜想Ⅲ成立。写出无色溶液B与硝酸中和反 应的化学方程式_________________。 |
③ | 若现象a、b均 为:产生白色沉淀 | 则猜想____成立。写出无色溶液B与硝酸钡溶液 反应的化学方程式______________。 |
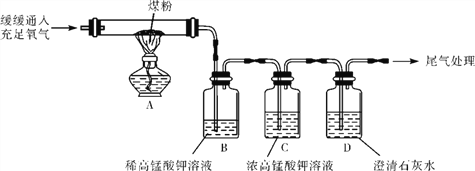
【题目】化学反应速率是衡量化学反应进行快慢的物理量,为了探究影响化学反应速率的因素,以过氧化氢分解为研究对象进行实验。各小组均可采用如图装置进行实验,记录收集10mL氧气的时间,实验室可供选择的试剂有:2.5%、5%、10%三种浓度的H2O2溶液、MnO2、CuO、红砖粉末。

A组:探究催化剂对化学反应速率的影响;
取5mL10%H2O2溶液,三次实验分别加人0.5gMnO2、红砖粉末、CuO进行实验,记录数据如下:
试剂 | MnO2 | 红砖粉末 | CuO |
t/s | 10 | 60 | 20 |
由此得出结论:MnO2、CuO对H2O2分解有催化作用,红砖粉末无催化作用。
(1)你认为该结论是否正确,为什么?_________________________________________。
(2)经过补充对比实验,证明红砖粉末有催化作用,则三者的催化效率由高到低的顺序为___________。
B组:探究浓度对化学反应速率的影响
甲同学:取10mL5%H2O2溶液,加入0.5gMnO2为催化剂,,进行实验,记录时间t1。
(3)乙同学:取10mL2.5%H2O2溶液,加入__________为催化剂,进行实验,记录时间t2。
实验结果:_______________________________________________________
结论:___________________________________________________________
【拓展探究】
(4)C组:探究____________对化学反应速率的影响。
各取10mL5%H2O2溶液和0.5gCuO为催化剂进行实验,两次实验分别将试管置于冰水浴和50℃热水浴,记录时间t3、t4。
(5)实验结果:_________________________;
结论:当反应物浓度和催化剂相同时,__________________________________。
(6)以上三组实验说明,影响化学反应速率的因素有:________________________。