题目内容
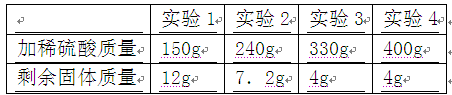
(10连云港)实验室里现有一包氯化镁和氯化钠的固体混合物样品,某同学取该样品12.8g,使之完全溶解在50g水中,再向其中加入40g20%的氢氧化钠溶液,恰好完全反应。求:(计算结果用百分数表示,保留到小数点后一位数字)
(1)样品中氯化镁的质量。
(2)反应后所得溶液中氯化钠的质量分数。
(1)样品中氯化镁的质量。
(2)反应后所得溶液中氯化钠的质量分数。
解:(1)设样品中氯化镁的质量为X
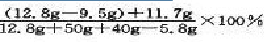
MgCl2 +2NaOH==Mg(OH)2↓+ 2NaCI (1分)
95 80 58 117
x 40g×20% y z
95:80="x:" 40g×20% x="9.5g "
(2)设反应后生成Mg(OH)2的质量为y,生成NaCI 的质量为z
80:58 = 40g×20%: y y="5.8g "
80:117 = 40g×20%: z z=11.7g
混合物中MgCl2的质量分数为:=95.0%
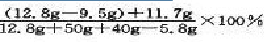
MgCl2 +2NaOH==Mg(OH)2↓+ 2NaCI (1分)
95 80 58 117
x 40g×20% y z
95:80="x:" 40g×20% x="9.5g "
(2)设反应后生成Mg(OH)2的质量为y,生成NaCI 的质量为z
80:58 = 40g×20%: y y="5.8g "
80:117 = 40g×20%: z z=11.7g
混合物中MgCl2的质量分数为:=95.0%
略

练习册系列答案
相关题目