题目内容
(10宁夏18).某钢铁冶炼厂购进一批铁矿石(主要成分是Fe2O3),为测定矿石中Fe2O3的质量分数,技术人员从矿石中取样品20g,恰好与219g质量分数为10%的盐酸完全反应(除Fe2O3外,盐酸不与其它成分反应)。计算:
(1)盐酸中溶质的质量是多少?
(2)样品中氧化铁的质量是多少?
(3)这批矿石中氧化铁的质量分数是多少?
(1)盐酸中溶质的质量是多少?
(2)样品中氧化铁的质量是多少?
(3)这批矿石中氧化铁的质量分数是多少?
解:(1)盐酸中溶质的质量:
219g×10%="21.9g " (1分)
(2)设样品中氧化铁的质量为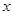
Fe2O3+6HCl=2FeCl3+3H2O (1分)
160 219
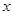 21.9
21.9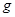 (1分)
(1分)
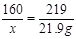 (1分)
(1分)
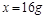 (1分)
(1分)
(3)这批矿石中氧化铁的质量分数:
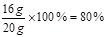 (1分)
(1分)
答:(略)
219g×10%="21.9g " (1分)
(2)设样品中氧化铁的质量为
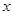
Fe2O3+6HCl=2FeCl3+3H2O (1分)
160 219
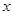 21.9
21.9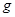 (1分)
(1分)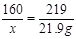 (1分)
(1分)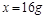 (1分)
(1分)(3)这批矿石中氧化铁的质量分数:
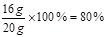 (1分)
(1分)答:(略)
略

练习册系列答案
相关题目