题目内容
【题目】水在生产生活中起着重要的作用。
①氢气燃烧是人们认识水组成的开始,化学方程式是___________________________。
电解水也可以证明水的组成化学方程式是________________________________
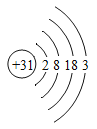
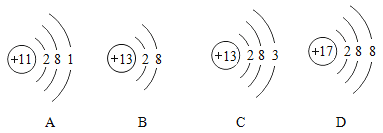
②自来水生产消毒过程中通入________,它与水反应生成盐酸和次氯酸(HClO),次氯酸中氯元素的化合价为_______。
③水在化学实验中的作用不可小觑。
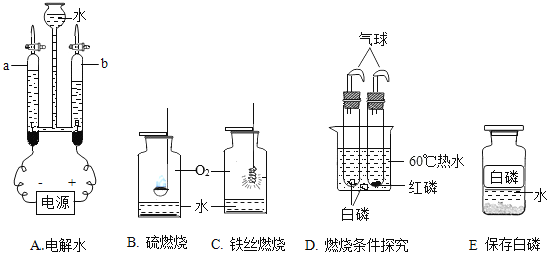
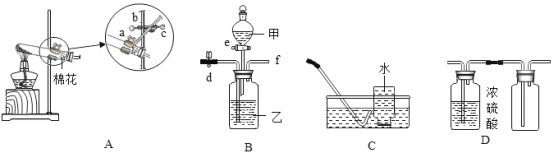
I.A中a、b管中气体的体积比约____________________,
II.B中燃烧的主要现象是_______________________________;
III.C中反应的化学方程式是_________________________,反应类型属于___________;
IV.D可以探究可燃物燃烧的条件是_______________________________;
V.上述实验中,水用来隔绝空气的是______________(填字母序号)。
【答案】2H2 + O2![]() 2H2O 2H2O
2H2O 2H2O![]() 2H2↑ + O2↑ Cl2(液氯/氯气) +1 1:2 明亮的蓝紫色火焰,生成刺激性气味的气体 3Fe+2O2
2H2↑ + O2↑ Cl2(液氯/氯气) +1 1:2 明亮的蓝紫色火焰,生成刺激性气味的气体 3Fe+2O2![]() Fe3O4 化合反应 与氧气(空气)接触、温度达到着火点 DE
Fe3O4 化合反应 与氧气(空气)接触、温度达到着火点 DE
【解析】
氢气和氧气点燃生成水,电解水生成氢气和氧气,硫在氧气中燃烧生成二氧化硫,铁丝在氧气中点燃生成四氧化三铁。
①氢气燃烧生成水,化学方程式是2H2 + O2![]() 2H2O,电解水生成氢气和氧气,化学方程式是2H2O
2H2O,电解水生成氢气和氧气,化学方程式是2H2O![]() 2H2↑ + O2↑。
2H2↑ + O2↑。
②自来水生产消毒过程中通入Cl2(液氯/氯气),次氯酸的化学式为HClO,次氯酸中氧元素的化合价为-2价,氢元素的化合价为+1价,设氯元素的化合价为x,则![]() ,x=+1,故氯元素的化合价为+1价。
,x=+1,故氯元素的化合价为+1价。
③I.电解水正极产生氧气,负极产生氢气,则a管生成氧气,b管生成氢气,故A中a、b管中气体的体积比约1:2。
II.硫在氧气中燃烧生成二氧化硫,B中燃烧的主要现象是产生明亮的蓝紫色火焰,生成刺激性气味的气体。
III.铁丝在氧气中点燃生成四氧化三铁,C中反应的化学方程式是3Fe+2O2![]() Fe3O4
Fe3O4
,反应符合多变一,属于化合反应。
IV.燃烧条件:物质是可燃物、达到可燃物的着火点、有氧气参与,D中有空气参与,红磷和白磷在60℃的温度下实验,故可以探究可燃物燃烧的条件是与氧气(空气)接触、温度达到着火点。
V.A中水是反应物,B中水用来吸收二氧化硫,C中水吸收热量,防止高温生成的熔融物炸裂瓶底,D中水用来隔绝空气,E中水用来隔绝空气,故水用来隔绝空气的是DE。

【题目】下表是NaCl、KNO3在不同温度时的溶解度,根据数据回答。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度 | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
(g/100g水) | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
①氯化钠的溶解度受温度变化的影响_____(填“很大”或“很小”)。
②50℃时,KNO3的溶解度_____(填“<”、“>”或“=”)NaCl的溶解度;向烧杯中加入100g水和49.0gKNO3固体配成50℃的溶液,再冷却到20℃,烧杯中析出固体的质量为_____g。
③KNO3中混有少量的NaCl,提纯的方法是_____(填“降温结晶”或“蒸发结晶”)。
④要比较NaCl和KNO3在水中的溶解性强弱,测定的数据可以是:相同温度下,等质量的溶质完全溶解达到饱和时所需水的质量;或_____。
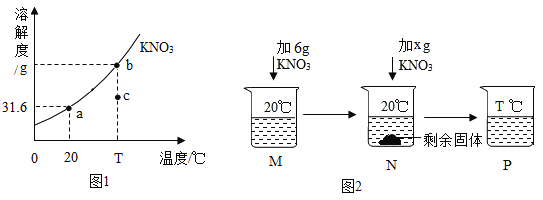
⑤如图是有关硝酸钾溶液的实验操作及变化情况,说法正确的是_____(填编号)。
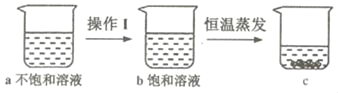
A 操作I一定是降温
B a与b的溶剂质量可能相等
C a与c的溶质质量一定相等
D b与c的溶质质量分数一定相等