题目内容
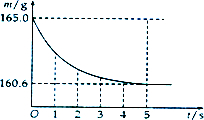
在烧杯中加入石灰石12.5g(所含杂质不与稀盐酸反应,也不溶于水),再加入100g稀盐酸恰好完全反应.反应过程中用精密仪器测得烧杯连同药品的总质量(m)与反应时间(t)的关系如图所示.烧杯连同药品的起始总质量为165.0g.试计算:
(1)完全反应时产生二氧化碳的质量.
(2)稀盐酸中溶质的质量分数.
(3)反应后过滤所得滤液中溶质的质量分数(精确到0.1%).
(1)完全反应时产生二氧化碳的质量.
(2)稀盐酸中溶质的质量分数.
(3)反应后过滤所得滤液中溶质的质量分数(精确到0.1%).

(1)放出二氧化碳的质量即为反应前后烧杯质量的变化,即165g-160.6g=4.4g.
答:产生的二氧化碳的质量为4.4g.
(2)设稀盐酸中溶质质量为x,生成氯化钙的质量为y,石灰石中碳酸钙的质量为w
CaCO3+2HCl=CaCl2+CO2↑+H2O
10073111 44
w xy4.4g
=
=
=
解之得:x=7.3g,y=11.1g,w=10g
则盐酸中溶质的质量分数=
×100%=7.3%
答:稀盐酸中溶质的质量分数为7.3%
(3)反应后所得溶液的质量=m(CaCO3)+m(盐酸)-m(CO2)=10g+100g-4.4g=105.6g
所以所得氯化钙溶液的质量分数=
×100%=10.5%
答:所得溶液的溶质的质量分数为10.5%
答:产生的二氧化碳的质量为4.4g.
(2)设稀盐酸中溶质质量为x,生成氯化钙的质量为y,石灰石中碳酸钙的质量为w
CaCO3+2HCl=CaCl2+CO2↑+H2O
10073111 44
w xy4.4g
| 73 |
| x |
| 111 |
| y |
| 44 |
| 4.4g |
| 100 |
| w |
解之得:x=7.3g,y=11.1g,w=10g
则盐酸中溶质的质量分数=
| 7.3g |
| 100g |
答:稀盐酸中溶质的质量分数为7.3%
(3)反应后所得溶液的质量=m(CaCO3)+m(盐酸)-m(CO2)=10g+100g-4.4g=105.6g
所以所得氯化钙溶液的质量分数=
| 11.1g |
| 105.6g |
答:所得溶液的溶质的质量分数为10.5%

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目