题目内容
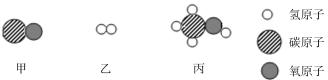
【题目】化学是在分子、原子层次上研究物质的性质、组成、结构与变化规律的科学.请你按要求填.
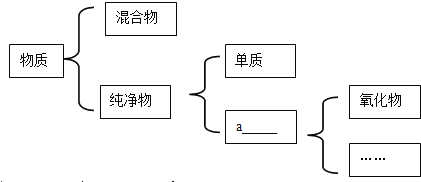
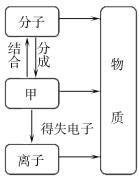
(1)图中a处应填写______.
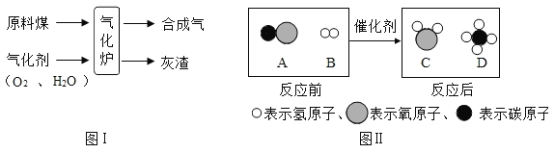
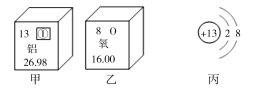
(2)有以下物质①空气、②氧气、③一氧化碳其中属于混合物的是(填序号)_____,属于单质的是(填序号)_____,它由(填粒子符号)______构成,填属于氧化物的是(填序号)_____,该物质能冶炼金属,利用了其______性.
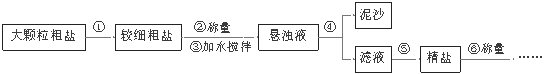
(3)氯化钠是由_________构成.(填粒子符号)
(4)结构决定性质,性质决定用途.元素的化学性质和________密切相关;稀有气体因为化学性质______决定了它可做保护气.
(5)用分子的观点解释日常生活中的现象
①100mL水和100mL酒精混合后体积小于200mL____________.
②品红在热水中扩散比冷水中快_______________.
【答案】化合物 ① ② O2 ③ 还原性 Na+ Cl- 原子最外层电子数 稳定 分子间存在间隔 温度越高分子运动越剧烈
【解析】
本题主要考察物质的分类以及化学符号的正确书写
(1)纯净物分为单质(只含有一种元素)和化合物(含有多种元素)。
(2)空气中含有多种物质是混合物;氧气是只含有一种元素纯净,属于单质;它由氧分子构成;一氧化碳是含有两种元素,其中一种是氧元素的纯净物,属于氧化物;一氧化碳具有还原性,可以冶炼金属。
(3)氯化钠由氯离子和钠离子构成。
(4)元素的化学性质与原子的最外层电子数由直接关系;稀有气体的化学性质稳定,可以做保护气。
(5)等体积的水和酒精混合,混合后的体积小于混合前体积之和,说明分子间有间隔;品红在热水中扩散比冷水中快,温度越高分子运动越剧烈。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】分析处理图表信息是学习化学的一种重要方法。下表是氯化钠和硝酸钾在不同温度下的溶解度,仔细阅读并回答下列问题。
温度/℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ |
氯化钠溶解度/g | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 |
硝酸钾溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
(1)氯化钠和硝酸钾的溶解度随温度变化趋势更大的是_____(填化学式)。
(2)20℃时,将40g硝酸钾固体加入到100g水中,充分搅拌后静置,得到的溶液是硝酸钾的_____(填“饱和”或“不饱和”)溶液。若将温度升高到50℃,所得溶液溶质的质量分数为_____(精确到0.1%)。