��Ŀ����
����Ŀ����������ͼ����Ϣ��ѧϰ��ѧ��һ����Ҫ�������±����Ȼ��ƺ�������ڲ�ͬ�¶��µ��ܽ�ȣ���ϸ�Ķ����ش��������⡣
�¶�/�� | 10�� | 20�� | 30�� | 40�� | 50�� | 60�� | 70�� | 80�� |
�Ȼ����ܽ��/g | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 |
������ܽ��/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
��1���Ȼ��ƺ�����ص��ܽ�����¶ȱ仯���Ƹ������_____���ѧʽ����
��2��20��ʱ����40g����ع�����뵽100gˮ�У���ֽ�����ã��õ�����Һ������ص�_____������͡������͡�����Һ�������¶����ߵ�50�棬������Һ���ʵ���������Ϊ_____����ȷ��0.1%����
���𰸡�KNO3 ���� 28.6%
��������
��1���Ȼ��ƺ�����ص��ܽ�����¶ȱ仯���Ƹ����������أ�
��2����20��ʱ������ص��ܽ����31.6�ˣ�100gˮ������ܽ�31.6�˵�����أ�����20��ʱ����40g����ع���Ͷ��100gˮ�У�����ܽ��ɵõ�����ر�����Һ�����¶����ߵ�50�棬������Һ���ʵ���������Ϊ![]() ��100%��28.6%��
��100%��28.6%��
�ʴ�Ϊ����1��KNO3����2�����ͣ�28.6%��

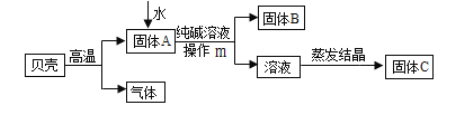
 �Ͻ�ƽ���Ȿϵ�д�
�Ͻ�ƽ���Ȿϵ�д� ����ѧ��Ӧ�����ϵ�д�
����ѧ��Ӧ�����ϵ�д�����Ŀ��������ʵ��ָ�������е�ˮ�������û������ˮ����Ҫ���õ��ǣ� ��
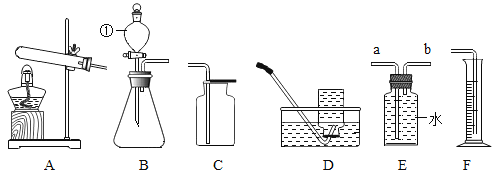
ʵ �� װ �� |
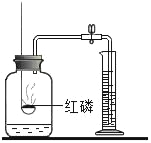
����������ȼ�� |
�ⶨ�������������� |
�ⶨ�������������� |
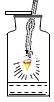
��˿��������ȼ�� |
���� | ����ƿ�е�ˮ�� ���շų������� | ����ƿ�е�ˮ�� ��������հ��� | ��Ͳ�е�ˮ�� ͨ��ˮ����ı仯�ó�������� | ����ƿ�е�ˮ�� ��ȴ�����������ֹ����ƿը�� |
A | B | C | D |
A. AB. BC. CD. D
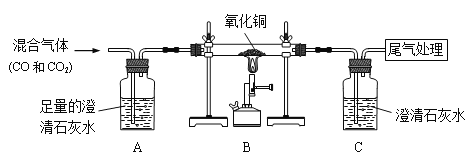
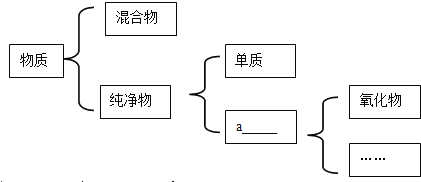
����Ŀ�������£�����ˮ�����ܷ�Ӧ����һ�ֳ��������������һ�����塣С���ܺ��棬�������ʵ��̽��������ˮ������Ӧ��IJ��
��1���Թ�β����һ��ʪ����Ŀ���� ��
��2��̽�����ɵ�������ʲô����ȼ�ŵ�ľ�����������ݣ��б��������Ժ��з�����Ʈ�����С�˵�����ɵ������� ��д���÷�Ӧ�Ļ�ѧ����ʽ ��
��3��̽���Թ���ʣ�����ɷ���ʲô��
���������ϡ�
�������������� | FeO | Fe2O3 | Fe3O4 |
��ɫ��״̬ | ��ɫ��ĩ | ����ɫ��ĩ | ��ɫ���� |
�ܷ������� | �� | �� | �� |
�����ᷴӦ | FeCl2+H2O | FeCl3+H2O | FeCl2+FeCl3+H2O |
��������֤��
�Թ���ʣ�����Ϊ��ɫ����ȫ��������������
����������衿
����һ��ʣ������� ���������ʣ������� ��
��ʵ��̽����
ʵ����� | ʵ�������� |
��ʵ����ۡ�����ˮ������Ӧ�Ļ�ѧ����ʽΪ ��