题目内容
【题目】氯碱工业以粗盐(主要成分是NaCl,此外还含有少量泥沙,CaCl2、MgCl2)为原料,生产氯气、氢气和氢氧化钠,模拟流程如下:
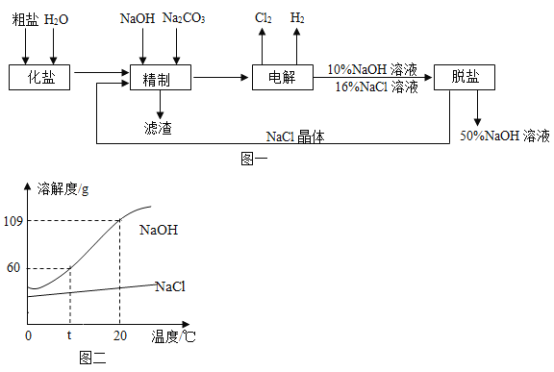
(1)图一精制过程中除去滤渣的操作是_____。
(2)图一流程中可以循环利用的物质是_____(填物质名称)。
(3)写出电解NaCl溶液的化学方程式:_____。
(4)图二为氢氧化钠和氯化钠的溶解度曲线,t℃时氢氧化钠的溶解度为_____,图一脱盐操作中除去氯化钠可以采用_____。(填“降温结晶”或“蒸发结晶”)法。
【答案】过滤 氯化钠晶体、氢氧化钠溶液 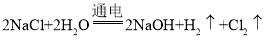 60g 蒸发结晶
60g 蒸发结晶
【解析】
(1)图一“精制”后得到固体和液体的混合物,分离固体和液体混合物的方法是过滤。故答案为:过滤;
(2)由流程图可知,脱盐后得到的氯化钠晶体可以作为精制步骤的原料,氢氧化钠溶液可作精制步骤的除杂物质。因此,图一流程中可以循环利用的物质是氯化钠晶体和氢氧化钠溶液。故答案为:氯化钠晶体、氢氧化钠溶液;
(3)由图一可知,氯化钠溶液通电时反应生成氢氧化钠、氢气和氯气,方程式为: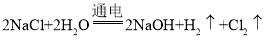 。故答案为:
。故答案为: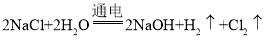 ;
;
(4)由图二可知,t℃时,氢氧化钠的溶解度为60g。氯化钠的溶解度受温度影响变化很小,氢氧化钠的溶解度受温度影响变化很大。因此,图一脱盐操作中除去氯化钠可以采用蒸发结晶的方法。故答案为:60g、蒸发结晶。

【题目】某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。请你计算:
(1)若要清洗1000kg的这种石油产品,需要_____kg的NaOH。
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。每处理1000kg这种产品,他们可以节约多少经费_____?请你写出具体的计算过程。工业级的NaOH和Ca(OH)2的最新市场批发价如下表:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 1.00 | 6.00 |
(3)请你在图中画出氢氧化钠和氢氧化钙处理1000kg该石油产品时,残余硫酸溶质的质量变化曲线;氢氧化钠用虚线表示,氢氧化钙用实线表示。_____(请你注明具体的坐标)