��Ŀ����
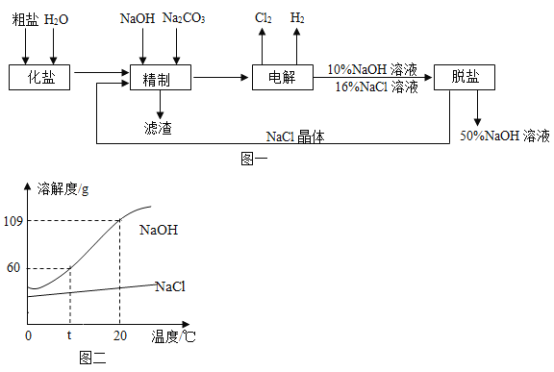
����Ŀ����ҵ������ͨ������������FeCl3���ʻ�ɫ��С��Ϊ�ⶨij��ҵ������HCl�ĺ�����������ʵ�飺ȡij��ҵ����100g���μ�һ����������������NaOH��Һ����ü���NaOH��Һ�������뷴Ӧ���ɵij���������ϵ��ͼ��ʾ��FeCl3��NaOH��Ӧ�Ļ�ѧ����ʽΪFeCl3+3NaOH�TFe��OH��3��+3NaCl����ش��������⡣
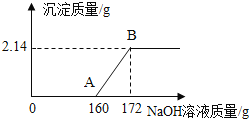
��1��A��ʱ����Һ�е�������______��
��2���ù�ҵ������HCl�����������Ƕ��٣�_____��д��������̣�
��3��ȡ100g�ù�ҵ����ϡ�ͳ�������������Ϊ10%��ϡ���ᣬ���ˮ______g��
���𰸡�NaCl��FeCl3 29.2% 192
��������
�⣺��1��A��ʱ����������������ǡ����ȫ��Ӧ����ʱ��Һ�е�������NaCl��FeCl3��
��2����ͼ��֪�����Ȼ�����Ӧ������������Һ������Ϊ172g-160g=12g��
�裺���ĵ��������Ƶ�����Ϊx

![]()
x=2.4g
����������Һ��������������![]()
�����ᷴӦ���������Ƶ�����Ϊ��160g��20%=32g
�裺�μӷ�Ӧ��������������Ϊy��
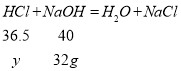
![]()
y=29.2g
�ù�ҵ������HCl������������![]() ��
��
��3�����ˮ������Ϊz
100g��29.2%=��100g+z����10%
z=192g��
��Ҫ��ˮ192g

����Ŀ����100g�Ȼ�þ��Һ�У����ϼ���һ��������������������������Һ��ʵ���������±���
����������Һ������/g | 5.6 | 11.2 | 22.4 | 33.6 |
���ɳ���������/g | 0.145 | 0.29 | 0.58 | 0.58 |
��1�����μ�����������Һ������Ϊ33.6gʱ��������Һ��pH_____������������=������������7��
��2��ѡ����������ݣ�������Ȼ�þ��Һ�����ʵ���������_____��
��3���������õ�����������Һ�����ʵ���������_____��