题目内容
【题目】金属材料在日常生活中的应用十分广泛,某化学兴趣小组对金属的相关知识进行了探究。
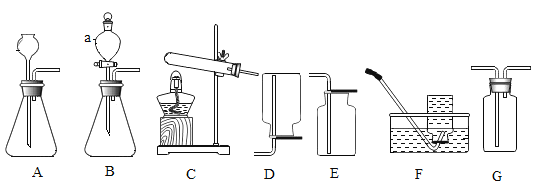
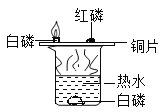
(1)该小组同学要用如图装置做一氧化碳还原氧化铁的实验并检验该反应的气体生成物。已知由一氧化碳发生装置得到的CO中混有杂质CO2和H2O。
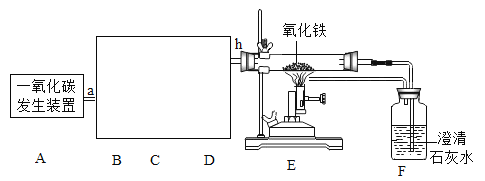
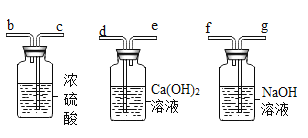
①请将下列装置接入到B、C、D位置中,装置中导管接口从左到右的连接顺序为:a→_________→h。
②F装置的双重作用是_____________。
③写出E装置中发生反应的化学方程式____________。
④实验开始时,使纯净的一氧化碳气体进入E装置一段时间后,再点燃E处酒精喷灯加热的目的是___________。
(2)某同学将一定量的锌粉加入到AgNO3、Cu( NO3 )2、Al(NO3)3的混合溶液中,充分反应后过滤,发现滤液为无色,向滤渣中滴加稀盐酸,没有气泡产生。
①根据现象判断滤渣的成分________。(填化学式)
②写出将锌粉加入混合溶液中发生反应的化学方程式________。(任写一个)
③猜想:滤液中的溶质为AgNO3、Zn( NO3)2、Al( NO3)3,请分析该猜想不合理的原因________。
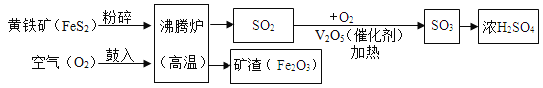
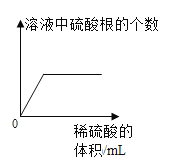
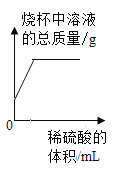
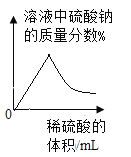
(3)为了测定某黄铜样品(铜锌合金)中铜的质量分数,称取10g样品放入烧杯中,加入100g稀硫酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为109.9g,请计算该样品中铜的质量分数________。
【答案】f→g→e→d→b→c 检验生成的CO2并除去未反应完的CO 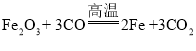 排尽装置内的空气,防止加热时发生爆炸 Ag和Cu
排尽装置内的空气,防止加热时发生爆炸 Ag和Cu ![]() [或
[或![]() ] 根据金属活动性顺序,锌先与AgNO3反应,反应完后再与Cu(NO3)2反应,当溶液中没有Cu(NO3)2时,则一定没有AgNO3。 67.5%
] 根据金属活动性顺序,锌先与AgNO3反应,反应完后再与Cu(NO3)2反应,当溶液中没有Cu(NO3)2时,则一定没有AgNO3。 67.5%
【解析】
(1)①CO中混有杂质CO2和H2O,故应先除去二氧化碳和水,再做一氧化碳还原氧化铁的实验,除杂时,应先用氢氧化钠溶液除去二氧化碳,而且洗气应“长进短出”,故a应连接f,然后用氢氧化钙溶液检验二氧化碳是否除尽,故g应连接e,最后用浓硫酸除去水,故d应连接b,故装置中导管接口从左到右的连接顺序为:a→f→g→e→d→b→c;
②F装置可检验E装置中是否有二氧化碳生成,同时将未反应完的一氧化碳在导管管口处点燃,除去未反应完的一氧化碳,故F装置的双重作用是检验生成的CO2并除去未反应完的CO;
③E装置中为一氧化碳与三氧化二铁在高温下反应生成铁与二氧化碳,其化学反应方程式为: ;
;
④一氧化碳属于可燃性气体,可燃性气体中混有一定量空气或氧气时,遇明火会发生爆炸,故实验开始时,先使纯净的一氧化碳气体进入E装置一段时间,排尽装置内的空气,再点燃E处酒精喷灯加热,故填:排尽装置内的空气,防止加热时发生爆炸;
(2)①将一定量的锌粉加入到AgNO3、Cu( NO3 )2、Al(NO3)3的混合溶液中,锌粉先和硝酸银反应生成硝酸锌和银,待硝酸银完全反应后,锌粉再和硝酸铜反应生成硝酸锌和铜,充分反应后,过滤,滤液为无色,说明硝酸铜已经完全反应,向滤渣中滴加稀盐酸,无气泡产生,说明锌粉已经完全反应,则滤渣的成分为Cu和Ag;
②将锌粉加入混合溶液中发生反应的化学方程式为:![]() [或
[或![]() ];
];
③锌粉会先和硝酸银反应生成硝酸锌和银,待硝酸银完全反应后,再和硝酸铜反应生成硝酸锌和铜,硝酸铜已经完全反应,说明硝酸银已经完全反应,滤液中的溶质不可能含有硝酸银;
(3)解:生成氢气的质量为:10g+100g-109.9g=0.1g;
设样品中铜的质量是x,则锌的质量为10g-x
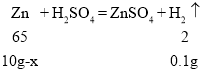
![]()
x=6.75 g
该样品中铜的质量分数为:![]()
答:样品中铜的质量分数为67.5%。

 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案