题目内容
【题目】以黄铁矿为原料,生产硫酸的简要流程如图:
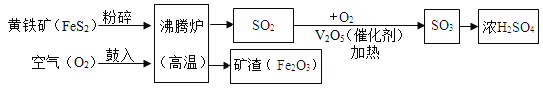
(1)黄铁矿中的元素一定含有_________。
(2)该生成流程中,生产设备不是敞开的、以防_________(填一种气体)泄漏造成空气污染。
(3)流程中SO2转化为SO3的反应属于化合反应,其化学方程式为__________。
(4)浓硫酸具有___________性,必须密封保存。
【答案】铁、硫 二氧化硫 2SO2+O2 2SO3 吸水性
2SO3 吸水性
【解析】
(1)黄铁矿和空气反应生成了二氧化硫和氧化铁,所以黄铁矿中的元素一定含有铁、硫;
(2)二氧化硫有毒,所以该生成流程中,生产设备不是敞开的,以防二氧化硫泄漏造成空气污染;
(3)二氧化硫和氧气在催化剂的作用下加热生成三氧化硫,化学方程式为:2SO2+O2 2SO3;
2SO3;
(4)浓硫酸有吸水性,必须密封保存。

 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案【题目】将25.6 g NaCl和MgCl2固体混合物完全溶于126 g水中配成溶液,再将200 g一定溶质质量分数的NaOH溶液不断加入该溶液中。充分反应后,测得的实验数据如下表。求:
实验次数 | 1 | 2 | 3 | 4 | 5 |
加入NaOH 溶液质量/g | 40 | 40 | 40 | 40 | 40 |
共生成沉 淀的质量/g | 2.9 | 5.8 | m | 11.6 | 11.6 |
(1)上表中m的值为多少。
(2)恰好完全反应时,所得溶液中溶质的质量分数。
【题目】某化学兴趣小组做木炭还原氧化铁的实验时,对反应后产生的气体成分进行了如下探究。
[提出问题]反应后的气体成分是什么?
[猜想假设]猜想1:该气体可能只是CO2猜想2:该气体可能只是CO
猜想3:_____。
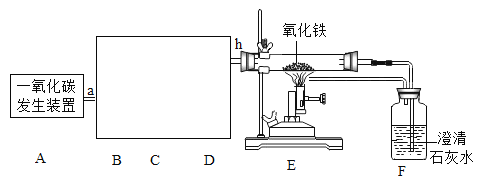
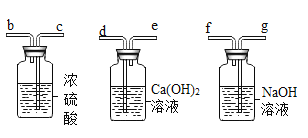
[设计实验]称取一定量的氧化铁和过量炭粉,在隔绝氧气的条件下完全反应,按照如图所示的实验操作连接装置。
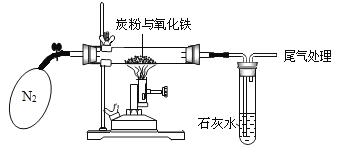
(1)加热前,先通入一段时间纯净且干燥的氮气,这样做的目的是_____。
(2)夹紧通氮气处的弹簧夹,加热一段时间后,观察到_____现象时,证明猜想2不成立。
(3)待反应结束后,应先_____,再_____,冷却至室温后,停止通入氮气,称量硬质玻璃管和固体的总质量,实验所记录的数据如下表。
氧化铁 | 炭粉 | 硬质玻璃管 | |
反应前质量(g) | 1.6 | 1 | 40 |
反应后质量(g) | 硬质玻璃管和固体总质量:41.88 | ||
[数据处理]生成物中碳元素和氧元素的质量比为_____。
[实验结论]根据上述数据处理分析得出猜想_____成立。
[交流反思]请设计检验硬质玻璃管反应后剩余的固体中有炭粉_____(写出操作及现象)。