题目内容
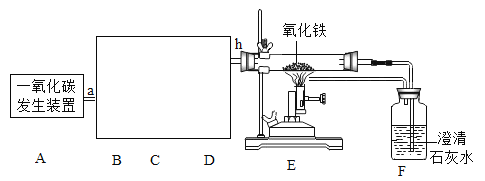
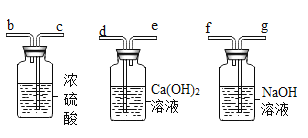
【题目】向硝酸银和硝酸铜的混合溶液中加入一定量的铝粉和锌粉,充分反应后过滤,得到滤渣和蓝色滤液。
(1)若滤渣中有红色固体,则反应后所得滤液中的溶质是什么____________?
(2)若向滤液中加入稀盐酸时有白色沉淀生成,写出向硝酸银和硝酸铜的混合溶液中加入一定量的铝粉和锌粉后发生反应的化学方程式____________。(写一个即可)
【答案】硝酸铜、硝酸锌、硝酸铝 ![]() 或
或![]()
【解析】
在硝酸银和硝酸铜的混合溶液中加入一定量的铝粉和锌粉,充分反应后过滤,得到滤渣和蓝色滤液,说明硝酸铜可能未参加反应或者部分参加反应,加入的铝粉和锌粉全部反应完。
(1)若滤渣中有红色固体,说明部分硝酸铜参加了反应,硝酸银全部被反应,则滤液中溶质为剩余的硝酸铜和反应生成的硝酸铝、硝酸锌。
(2)若向滤液中加人稀盐酸时有沉淀生成,说明滤液中有硝酸银存在,铝粉和锌粉全部和硝酸银发生反应,被置换出的金属只有银,该过程中涉及的是铝和硝酸银反应产生硝酸铝和银:![]() ,以及锌和硝酸银反应生成硝酸锌和银:
,以及锌和硝酸银反应生成硝酸锌和银:![]() 。
。

【题目】KNO3和NaCl在不同温度时的溶解度如下图所示,请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | |
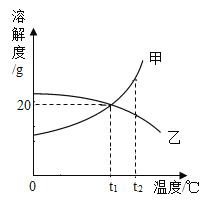
(1)依据上表数据,绘制出KNO3和NaCl的溶解度曲线如图所示:
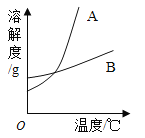
图中能表示KNO3溶解度曲线的是_____(选填“A”或“B”)
(2)由表中数据分析可知,20℃时40gNaC1溶解在50g水中得到溶液_____g。
(3)硝酸钾中含有少量氯化钠时,可通过_____(选填“蒸发结晶”或“降温结晶”)的方法提纯。
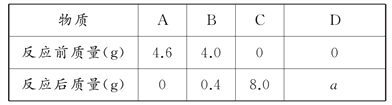
【题目】将25.6 g NaCl和MgCl2固体混合物完全溶于126 g水中配成溶液,再将200 g一定溶质质量分数的NaOH溶液不断加入该溶液中。充分反应后,测得的实验数据如下表。求:
实验次数 | 1 | 2 | 3 | 4 | 5 |
加入NaOH 溶液质量/g | 40 | 40 | 40 | 40 | 40 |
共生成沉 淀的质量/g | 2.9 | 5.8 | m | 11.6 | 11.6 |
(1)上表中m的值为多少。
(2)恰好完全反应时,所得溶液中溶质的质量分数。