题目内容
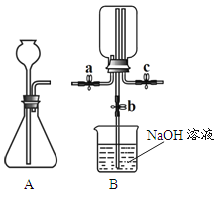
【题目】下图是实验室组装制取气体装置时,可能用到的仪器,回答问题。
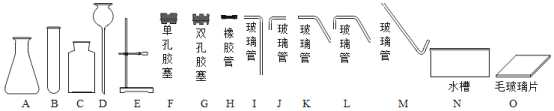
(1)写出仪器B的名称__________;
(2)实验室用大理石和稀盐酸制取CO2,发生反应的化学方程式:______,组装制取装置时,除选用A、C、G、H、L、N、O外,还需选用的仪器是__________;
(3)制取CO2气体的装置,还可用于H2O2溶液和MnO2混合制O2,但不能用于以KMnO4为原料制O2。则组装制取气体装置时,需考虑反应物状态、_________和气体的性质。
【答案】试管 CaCO3+2HCl=CaCl2+CO2↑+H2O D、M 反应条件
【解析】
稀盐酸和碳酸钙生成氯化钙、水和二氧化碳。
(1)仪器B的名称试管。
(2)实验室用大理石和稀盐酸制取CO2,发生反应是稀盐酸和碳酸钙生成氯化钙、水和二氧化碳,反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O,实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳密度比空气大,溶于水,组装制取装置时因为已经选择了A、C、G、H、L、N、O,说明采用了排水法收集,则还需选用的仪器是D、M。
(3)制取CO2气体的装置,还可用于H2O2溶液和MnO2混合制O2,反应均在常温下进行,高锰酸钾制取氧气,需要加热,但不能用于以KMnO4为原料制O2。则组装制取气体装置时,需考虑反应物状态、反应条件和气体的性质。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
纯净物 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
反应前质量/g | 2.3 | 4 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 2.2 | 2.7 | 待测 |
A.反应后X的质量为1.5g B.X中一定含有碳元素和氧元素
C.X中一定含有碳元素和氢元素 D.X中两种元素的质量比是1:1
【题目】兴趣小组的同学对金属的某些性质进行相关探究。
(实验回顾)
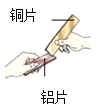
(1)如图所示,将两块金属片进行相互刻划。该实验的目的是_____。
(2)用坩埚钳夹住一块铝箔在酒精灯上加热至较高温度时,轻轻摇晃,发现熔化的铝不滴落,好像有一层膜兜着(资料:铝的熔点660℃,氧化铝的熔点2054℃。)。请解释原因_____。
(实验探究)铝与氯化铜溶液的反应

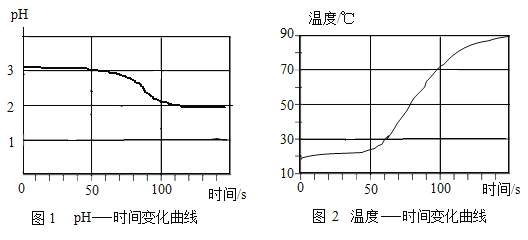
将打磨过的铝片放在15%氯化铜溶液中,观察到铝片表面逸出大量无色气体,且附着红色物质,过一段时间还有白色沉淀产生。利用温度传感器和pH传感器监测实验过程中的相关数据(如图所示)。
(实验反思)
(1)写出生成红色物质的化学方程式为_____。
(2)结合图1分析,铝和氯化铜溶液反应生成的无色气体是_____(填名称)。
(提出问题)白色沉淀的化学成分是什么?
(查阅资料)
①氢氧化铝、氯化亚铜(CuCl)均是难溶于水的白色固体。
②CuCl可与浓氨水反应生成无色的Cu(NH3)2+和Cl—。
③Cu(NH3)2+在空气中易被氧化变为蓝色;Cl—可与硝酸银溶液反应,产生白色沉淀。
(实验方案)将上述实验中产生的沉淀过滤出来,并洗涤干净后,加入浓氨水,沉淀部分溶解得到无色溶液,将无色溶液分为两份,进行实验。
操作步骤 | 实验现象 | 实验结论 |
用试管取其中一份溶液,滴加适量AgNO3溶液 | _____ | 该溶液中含有Cl— |
将另一份溶液置于空气中一段时间 | _____ | 该溶液中含有Cu(NH3)2+ |
(实验结论)通过实验可以确定,该白色固体是CuCl。
(反思与评价)
(1)小组同学将Cu粉与15%CuCl2溶液混合,没有观察到白色沉淀。在老师的启发下,结合图2“温度-时间变化曲线”,对实验进行改进,确证了Cu与CuCl2溶液反应生成CuCl。请你写出改进后的实验方案是_____。
(2)经过讨论CuCl是Cu与CuCl2化合反应生成。
(思维拓展)
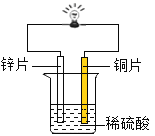
(1)金属锌、铜和稀硫酸构成化学电池(如图)。观察到铜片表面有气泡(H2),小电珠发光、烧杯中溶液始终无色。下列关于实验的分析不正确的是_____(填序号)。
A 铜与稀硫酸发生了置换反应
B 铜的金属活动性变得比锌强
C 烧杯中溶液的pH会逐渐增大
D 该装置将电能转化为化学能
(2)某工厂化验室用20%NaOH溶液来中和上图实验前烧杯中的H2SO4,共消耗NaOH溶液20g,反应后的溶液呈中性,则上图烧杯中原来所含H2SO4的质量为_____(写出计算过程)。