题目内容
【题目】金属在生产、生活中应用广泛。
(1)将铝块制成铝箔是利用了铝的___________。
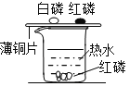
(2)铁制品锈蚀的过程,实际上是铁与空气中的______________等发生化学反应的过程。请写出稀硫酸去除铁锈的化学方程式___________。而铝具有很好的抗腐蚀性,原因是_________。
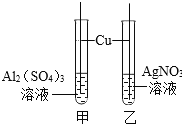
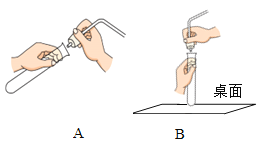
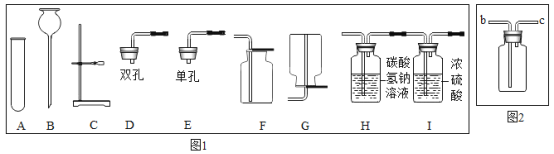
(3)小明设计了如图的实验方案,通过观察到_________的现象,得出三种金属的活动性由强到弱的顺序为铝>铜>银。写出试管乙中反应的化学方程式_________。
【答案】延展性 ![]()
![]() 铝易在空气中形成一层致密的氧化膜 甲中无明显现象,乙中铜丝表面有银白色固体析出,溶液由无色变成蓝色
铝易在空气中形成一层致密的氧化膜 甲中无明显现象,乙中铜丝表面有银白色固体析出,溶液由无色变成蓝色 ![]()
【解析】
(1)铝块能制成铝箔是利用了铝的延展性;故填:延展性;
(2)铁的锈蚀实际是铁与空气中的水和氧气共同作用的结果,铁锈的主要成分是氧化铁,与硫酸反应生成硫酸铁和水;铝易和氧气反应生成致密氧化铝保护膜,故填:水和氧气;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;铝易和氧气反应生成致密氧化铝保护膜;
(3)甲试管没有变化,乙试管中的铜丝表面覆盖一层银白色物质,溶液变成了蓝色,这是因为铜与硝酸银反应生成银和硝酸铜,实验这说明了铝的活动性大于铜,铜的活动性大于银;故填:甲中无明显现象,乙中铜丝表面有银白色固体析出,溶液由无色变成蓝色;Cu+2AgNO3=2Ag+Cu(NO3)2。

 阅读快车系列答案
阅读快车系列答案【题目】日常生活中常采用煮沸方法将硬水软化。这种方法一定可靠吗?
(查阅资料)水的硬度由水中所溶解的可溶性钙镁化合物引起的,硬水中所溶解的钙镁化合物可分为两类:钙、镁的碳酸氢盐,如Ca(HCO3)2等;钙、镁的硫酸盐或氯化物,如CaCl2等,一般所说水的硬度是由上述两类化合物引起的。
(设计并实验)小明为方便研究准备了碳酸氢钙溶液和氯化钙溶液来代表两类不同的钙、镁化合物。
实验编号 | 实验操作 | 实验现象 |
① | 分别取5mL的碳酸氢钙溶液和氯化钙溶液于A. B两支试管中,同时加热 | A试管中产生大量气泡,有沉淀产生,B试管无明显现象 |
② | 在上述实验后,分别滴加4滴肥皂水,振荡 | A试管中有大量的泡沫,B试管中泡沫较少 |
(得出结论)
(1)煮沸实际上只能降低____________所引起的水的硬度。实验中A试管中碳酸氢钙分解除产生沉淀外,还生成了另外两种氧化物,请写出该反应的化学方程式_______________。
(评价与反思)
①小芳同学提出,若向碳酸氢钙溶液中滴加少量酚酞溶液,溶液变为红色,则说明__________________。
②在实验室中一般可通过___________来降低水的硬度,硬水会给我们的生活和生产带来很多危害,请写出一种___________________________________________________。
(实验拓展)向澄清石灰水中持续通CO2气体,会得到Ca(HCO3)2溶液。利用pH传感器测定在此操作过程中pH变化曲线如图所示:请写出两条现象或结论。
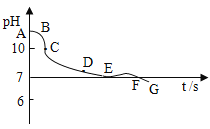
①______________________________________。
②______________________________________。