题目内容
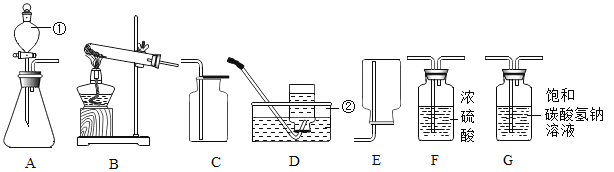
【题目】为测定某黄铜矿(主要成分是CuFeS2,含少量SiO2)的纯度,如图所示进行实验:称取一定质量样品,研细后放入装置中充分燃烧,反应方程式为:6CuFeS2+19O2![]() 6CuO+2Fe3O4+12SO2。实验前、后称量装置D的质量,差值为二氧化硫的质量,再根据方程式计算出 的质量,从而确定黄铜矿的纯度。(装置气密性良好;SiO2 不参与反应)资料:SO2+2NOH=Na2SO3+H2O;2SO2+O2+4NaOH=2Na2SO4+2H2O。
6CuO+2Fe3O4+12SO2。实验前、后称量装置D的质量,差值为二氧化硫的质量,再根据方程式计算出 的质量,从而确定黄铜矿的纯度。(装置气密性良好;SiO2 不参与反应)资料:SO2+2NOH=Na2SO3+H2O;2SO2+O2+4NaOH=2Na2SO4+2H2O。
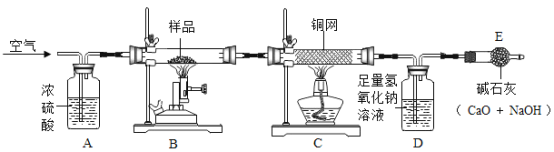
(1)将样品研细的主要目的是________。
(2)装置A中,浓硫酸的作用是________;装置A的另一个作用是______。
(3)样品煅烧充分后应继续通一会儿空气,是为了______。
(4)装置C的作用是_______,为了提高测定结果的精确度,该实验还需做的一个改进是______。
【答案】增大反应物接触面积,反应更快、更充分 吸收空气中的水蒸气 通过导管口产生气泡的速率控制通入空气的速率 使反应生成的二氧化硫完全被D装置吸收 除去二氧化硫中的氧气 在A装置前添加一个盛有足量氢氧化钠溶液的洗气瓶
【解析】
(1)将样品研细的主要目的是增大反应物接触面积,反应更快、更充分.
故填:增大反应物接触面积,反应更快、更充分.
(2)装置A中,浓硫酸的作用是吸收空气中的水蒸气;
装置A的另一个作用是通过导管口产生气泡的速率控制通入空气的速率.
故填:吸收空气中的水蒸气;通过导管口产生气泡的速率控制通入空气的速率.
(3)样品煅烧充分后应继续通一会儿空气,是为了使反应生成的二氧化硫完全被D装置吸收.
故填:使反应生成的二氧化硫完全被D装置吸收.
(4)装置C的作用是除去二氧化硫中的氧气;
为了提高测定结果的精确度,该实验还需做的一个改进是:在A装置前添加一个盛有足量氢氧化钠溶液的洗气瓶,把通入空气中的二氧化碳除去,使实验结果更准确.
故填:除去二氧化硫中的氧气;在A装置前添加一个盛有足量氢氧化钠溶液的洗气瓶.

 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案【题目】某化学课堂上同学们进行酸、碱、盐知识的探究,请你参与其中并认真填写空格.
(学生实验)将二氧化碳分别通入石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象.
(学生板演)澄清石灰水变浑浊的原理________________(用化学方程式表示)。
(提出问题)二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
(猜想假设)猜想①:两者发生了化学反应;猜想②:两者没有发生化学反应。
(实验探究)(1)小华设计了如图所示的A、B两个实验.
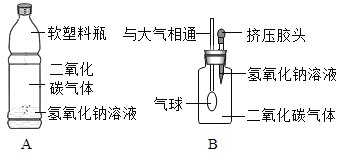
实验现象:A中软塑料瓶変瘪,B中___________。
(2)小红认为小华的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低.小明同学却对此提出质疑,他认为小华的实验不严谨,其理由是___________,要得到科学严谨的结论,仍利用该装置,补做的对比实验是_______________。
(注意:若正确回答(3)奖励4分,化学总分不超过60分)
实验步骤 | 实验现象 | 实验结论 |
向B实验后的溶液中加入______________ | __________________ | 证明了二氧化碳和氢氧化钠溶液反应 |
(3)小宁设计的是通过检验生成物来验证猜想,请帮她填写实验报告。
(实验结论)二氧化碳和氢氧化钠溶液反应
(反思拓展)通过此实验探究,我们发现,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是__________________。
【题目】某同学查阅资料得知,实验室常用电石(主要成分CaC2)与水反应制取乙炔(C2H2),反应的化学方程式为:CaC2+H2O=Ca(OH)2+ C2H2![]() (电石中的杂质不溶于水且不参与反应)。在实验室中,该同学把一定量的CaC2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液,并对滤液的成分进行探究。
(电石中的杂质不溶于水且不参与反应)。在实验室中,该同学把一定量的CaC2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液,并对滤液的成分进行探究。
[提出问题]:滤液中溶质的成分是什么?
[猜想与假设]:猜想一:NaOH、Na2CO3
猜想二:NaOH
猜想三:NaOH、__________(将猜想三补充完整)
[分析与推理]:
反应后滤液中一定存在的溶质是__________(填化学式,下同),可能存在的溶质是______和______。对可能存在的溶质,需进一步实验验证。
[设计并实验]:
实验序号 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量滤液于试管中,向其中加入过量稀盐酸 | 无气泡产生 | 猜想_____不成立 |
实验二 | 另取少量滤液于试管中,向其中滴入适量碳酸钠溶液 | _________________ | 猜想三成立,发生反应的化学方程式为_______ |
[拓展延伸]:
若向CuCl2溶液中加入少量CaC2,充分反应,可观察到有气泡产生,同时出现蓝色的沉淀。写出产生蓝色沉淀的这一步反应方程式 ________________________。实验室保存电石应注意______。
【题目】为研究物质的溶解现象进行了如下实验(20℃),现象如下图所示(水的密度为1 g/cm3):
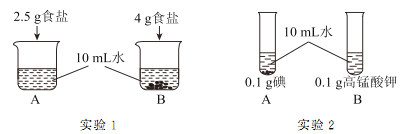
(1)实验1一定为饱和溶液的是_______(填序号)。
(2)实验2观察到碘几乎不溶解,高锰酸钾全部溶解,该实验可得出的结论是_______
(3)以下是氯化钠和高锰酸钾的溶解度表。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
高锰酸钾 | 2.8 | 4.3 | 6.4 | 9.0 | 12.6 | 18.0 | 22.1 | |
将50℃的高锰酸钾饱和溶液和氯化钠的饱和溶液冷却到20℃时,氯化钠溶液的溶质质量分数____<填“>”“<”或“=”)高锰酸钾溶液的溶质质量分数。
【题目】某研究性学习小组在”利用燃碳法测定空气中氧气的体积分数”的实验时(如图),发现个现象:用氢氧化钠溶液吸收生成的二氧化碳后,进入氧气瓶中水的体积分数仍然小于1/5。

(提出问题)是什么原因导致测量不准确呢?
(猜想与假设)他们分别作了如下猜想:
甲同学:可能是木炭取的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气。
(探究一)
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,都认为_____同学的猜想不合理。
(查阅资料)木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数分别高达14.0%,8.0%和16.0%
(进行实验)乙同学又利用上述装置设计了如下实验,请你填写下表:
实验步骤 | 实验现象 | 实验讨论 |
①将足量木炭点燃,迅速插入集气瓶中 | _____ | 木炭燃烧没有消耗完集气瓶中的氧气 |
②待装置冷却后,将燃着的________(填“棉花”或蜡烛)再伸入集气瓶中 | _____ |
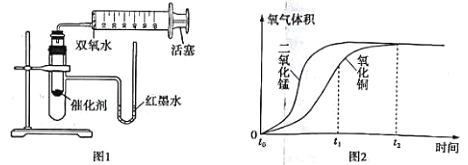
(实验反思)小明从木炭燃烧产物的角度猜想还可能是生成了_____导致测量结果小于1/5;于是用注射器抽取集气瓶内的气体做了图2所示的实验,当观察到澄清石灰水变浑浊,可证明小明的猜想成立,则该现象涉及的化学方程式为_____,该实验中没有观察到氧化铜粉末变红的原因可能是_____
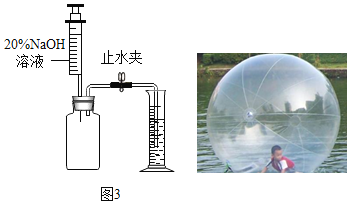
(拓展迁移)若要测量“水上步行球”内空气中二氧化碳的体积含量,利用图3装置,若集气瓶中收集的“水上步行球”内空气样品的体积为500mL,加入足量的氢氧化钠溶液充分振荡后,打开止水夹后量筒中的水流入集气瓶中5mL,则球内空气中CO2的体积含量是_____