题目内容
【题目】为研究物质的溶解现象进行了如下实验(20℃),现象如下图所示(水的密度为1 g/cm3):
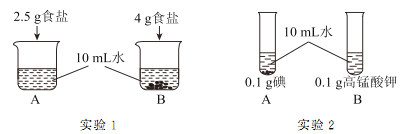
(1)实验1一定为饱和溶液的是_______(填序号)。
(2)实验2观察到碘几乎不溶解,高锰酸钾全部溶解,该实验可得出的结论是_______
(3)以下是氯化钠和高锰酸钾的溶解度表。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
高锰酸钾 | 2.8 | 4.3 | 6.4 | 9.0 | 12.6 | 18.0 | 22.1 | |
将50℃的高锰酸钾饱和溶液和氯化钠的饱和溶液冷却到20℃时,氯化钠溶液的溶质质量分数____<填“>”“<”或“=”)高锰酸钾溶液的溶质质量分数。
【答案】B 20℃时,碘和高锰酸钾在水中的溶解性不同 >
【解析】
(1)实验1:一定为饱和溶液的是B,因为B中食盐有剩余,不能继续溶解食盐。
(2)实验2,观察到碘几乎不溶解,高锰酸钾全部溶解,说明20℃时,碘和高锰酸钾在水中的溶解性不同。
(3)由氯化钠和高锰酸钾的溶解度表,将50℃的高锰酸钾饱和溶液和氯化钠的饱和溶液冷却到20℃时,均会析出晶体,所得溶液均为饱和溶液,20℃时氯化钠的溶解度大于高锰酸钾的溶解度,饱和溶液中溶质质量分数=![]() ×100%,则冷却到20℃时,氯化钠溶液的溶质质量分数>高锰酸钾溶液的溶质质量分数。
×100%,则冷却到20℃时,氯化钠溶液的溶质质量分数>高锰酸钾溶液的溶质质量分数。
故答案为:
(1)B;
(2)20℃时,碘和高锰酸钾在水中的溶解性不同;
(3)>。

 名校通行证有效作业系列答案
名校通行证有效作业系列答案【题目】安琪同学为探究铁制品锈蚀的条件,进行如下实验:
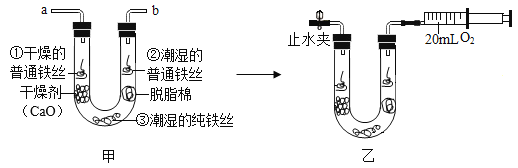
步骤1:利用图甲所示装置,将干燥的O2从导管a通入U形管(装置气密性良好,药品如图所示);待U形管内充满O2后,在导管b处连接一活塞推至底部的注射器收集20mLO2后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形管内的铁丝其现象如下表所示。
观察对象 | 现 象 |
①干燥的普通铁丝 | 无明显变化 |
②潮湿的普通铁丝 | ___________ |
③潮湿的纯铁丝 | 无明显变化 |
(1)步骤1中,检查U形管内是否已充满O2的方法是____________。
(2)铁制品锈蚀的条件之一是需要O2,在此实验中能支持此条件的证据是_____。
(3)通过对比实验现象,此实验还可得出铁制品锈蚀的条件是_________和__________。
(4)雨后郊外的路比较泥泞,如果你的交通工具是自行车,你回来进行清洗后,采取的防锈措施是: _______(填字母)
A.立即晾晒干 B.涂油漆 C.链条传动部件涂上油