题目内容
【题目】下面是某化学兴趣小组的同学对氢氧化钠部分性质的探究过程:
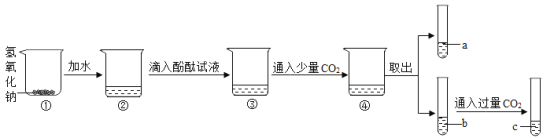
(1)用手触摸②的烧杯外壁,感觉发烫,这是由于氢氧化钠固体溶于水时会_______(填“吸热”或“放热”),③中的溶液显_______色.
(2)从③到④溶液的颜色变化不明显,说明④中的溶液呈______性(填“酸”或“碱”).
(3)c溶液和a溶液对比,c溶液颜色更浅.
(提出问题)为什么继续通入过量的二氧化碳气体溶液颜色会更浅?
(查阅资料)(1)Na2CO3+CO2+H2O==2NaHCO3 (2)Ca(NO3)2溶液与NaHCO3溶液不反应
(设计实验)
实验操作 | 实验现象 | 实验结论 |
取少量c溶液滴入稀盐酸 | ____ | 溶液中含较多的CO32﹣或HCO3﹣ |
另取少量c溶液滴入硝酸钙溶液 | 无明显现象 | 溶液中没有大量的____离子 |
(实验结论)根据甲、乙两个实验得出的结论,写出甲实验中发生反应的化学方程式:_____________________________.
(实验反思)同种反应物在不同的条件下发生化学反应时,可能得到不同的产物.如:碳在氧气中燃烧可以生成________或________.
(实验拓展)106g10% Na2CO3溶液与Ca(NO3)2完全反应生成沉淀 ______g
【答案】放热 红 碱 有大量气泡产生 碳酸根 NaHCO3+HCl=NaCl+H2O+CO2↑ 二氧化碳 一氧化碳 10
【解析】
(1)氢氧化钠固体溶解于水放热、氢氧化钠的溶液呈碱性,能使酚酞溶液变红;
(2)溶液颜色仍显红色,说明二氧化碳和氢氧化钠反应后的溶液仍然显碱性;
(3)[设计实验]含有碳酸根离子或是碳酸氢根离子,则加入盐酸会产生气泡,加入硝酸钙无明显现象,说明溶液中不存在碳酸根离子,否则将产生白色沉淀;
[实验结论]根据实验得出结论溶液中的溶质为碳酸氢钠,方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑;
[实验反思]很多物质在不同条件下会产生不同的产物,碳在氧气充足的时候生成二氧化碳,在氧气不足的时候生成一氧化碳;
[实验拓展]设106g10% Na2CO3溶液与Ca(NO3)2完全反应生成沉淀的质量为x,106g10% Na2CO3溶液中碳酸钠的质量=106g×10%=10.6g,
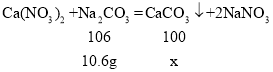
![]()
x=10g。

 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案【题目】鸡量主要由蛋壳、蛋壳膜、蛋白、蛋黄等几个部分组成,其中蛋壳的主要成分是CaCO3,里一层蛋壳膜。化学活动兴趣小组的同学开了以下探究活动:
(提出问题)蛋壳中的 CaCO3含量是多少?
(查阅资料)
a、蛋壳经过科学检测其中含CaCO3的质量分数的为82%~85%,含蛋白质质量分数的14-17%
b、蛋壳膜中蛋白质含量的为90%~93%。
c、Ba(OH)2是一种碱,化学性质与Ca(OH)2相似。
(设计方案)
方案一:用“灼烧法”,将该蛋壳放在空气中充分灼烧并采集相关数据进行测定。
方案二:用“酸处理法”,将蛋壳与稀盐酸反应后再进行吸收转变为碳酸钡进行测量处理。
(进行实验)
方案一:称取12.0g蛋壳研磨成粉末置于通风橱中,灼烧至质量不再减少,再称量剩余固体的质量为7.16g
方案二:用图2所示的连接实验装置。称取12g蛋壳样品进行实验(假设其他成分均不与HCI反应,装置内试剂均足量。)
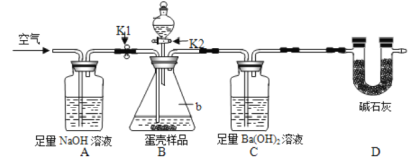
(实验步骤)
①按如图连接好装置后,并____________;
②向B装置中加入蛋壳样品后,先通入一会儿空气;
③关闭K1,打开K2,向蛋壳样品中滴入10%的盐酸,直到________为止;
④关闭K2,打开K1,再缓缓通入空气一会儿,至装置C中不再产生沉淀为止;
⑤将装置C中的固液混合物进行过滤、洗涤、烘干后称量其质量;
⑥重复上述实验
(数据处理)
方案一:产生的CO2质量_______g,蛋壳中CaCO3的质量分数为_______。(保留一位小数)
方案二:重复3次实验,记录数据如下:
实验次数 | 第1次 | 第2次 | 第3次 |
装置C中沉淀质量(/g) | 19.68 | 19.75 | 19.67 |
方案二中重复进进行实验的目的__________;生成沉淀的化学方程式是_________。实验测得蛋壳中的CaCO3的质量分数为________。
(评价反思)
(1)方案二中装置D的作用是_________。
(2)方案一测定值与科学检测的数据有较大误差,主要原因是________。
【题目】气体的实验室制取是初中化学重要的实验,根据下列提供的装置回答问题。
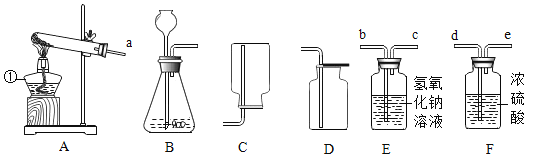
(1)装置A中标号①仪器的名称是_____。
(2)实验室制取二氧化碳的化学方程式为_____。
(3)制取并收集干燥的二氧化碳,应选用的装置有_____(选填字母)。
(4)检验二氧化碳是否收集满的方法是_____。
(5)固体碳酸氢钠受热能分解,产物为碳酸钠、水和二氧化碳,可利用装置A、E、F分析碳酸氢钠受热分解的情况。
①写出碳酸氢钠受热分解的化学方程式:_____。
②装置A、E、F中导管连接的顺序是_____(填小写字母)。
③部分实验数据见下表。其中x的值为_____。
装置 | 装置E | 装置F |
实验前的质量/g | 210.0 | 201.2 |
实验后的质量/g | x | 20.3.0 |
【题目】小华同学参加野炊活动,在整理调味料时不小心将一瓶醋打翻,醋洒在火炉旁的一堆草木灰上,发现有大量的气泡生成。激发了兴趣,于是他决定与学习小组的同学,对草木灰的成分进行探究。
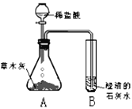
(探究活动1)根据所学知识,同学们猜想草木灰中含有能与酸反应产生气体的盐类物质,于是,设计并进行如右图所示的实验。
[现象] 观察到锥形瓶A中有大量的气泡冒出,试管B中澄清的石灰水变浑浊。
[推断] 试管B 中有关反应的化学方程式为 _______________。
[结论] 草木灰中一定含有_________(选填“硫酸盐”、“碳酸盐”或“硝酸盐”)。
(探究活动2)同学们认为还必须对草木灰中存在的盐类物质中所含的金属元素进行探究。
[资料摘要]
Ⅰ.多种金属化合物在灼烧时,产生的火焰呈现各种特殊的颜色,如:
化合物所含金属元素 | 钙元素 | 钾元素 | 铜元素 |
灼烧产生火焰颜色 | 砖红色 | 紫色(透过蓝色钴玻璃片) | 绿色 |
Ⅱ.碳酸钾与碳酸钠、碳酸氢钾与碳酸氢钠化学性质相似;碳酸氢钠性质不稳定,受热易分解。
(1)同学们在老师的指导下,取草木灰样品在火焰上灼烧,透过蓝色钴玻璃片观察到火焰呈__色,由此得出草木灰含有钾元素的结论。
(2)综合上述探究结果,进一步猜测草木灰中含有的钾盐是:a. KHCO3 b.K2CO3 c._____。
(3)小红认为上述猜测_____是错误的。理由是草木灰经柴草燃烧而成,_______。
(4)请你写出上述“探究活动1”中,锥形瓶A 内发生的一个反应的化学方程式:_________。简述草木灰的用途之一_______。 老师指出:草木灰成分复杂,其中所含其它成分的探究有待同学们后续进行。