题目内容
【题目】甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是
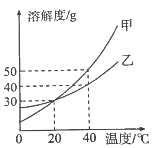
A.40℃时,甲的饱和溶液中溶质与溶剂的质量比为1∶2
B.20℃时,甲、乙溶液中溶质的质量分数相同
C.将40℃的甲、乙饱和溶液降温至20℃,甲析出的晶体比乙多
D.将20℃的甲、乙饱和溶液升温至40℃,所得溶液的溶质质量分数为甲大于乙
【答案】A
【解析】
A、40℃时,甲的饱和溶液中溶质与溶剂的质量比=50g:100g=1:2;故选项正确。
B、20℃时,甲、乙溶液中溶质的溶解度相同,但没有说明是饱和溶液,因此溶质质量分数不一定相同;故选项错误。
C、若是溶液的质量相同,则将40℃的甲、乙饱和溶液降温至20℃,甲析出的晶体比乙多,若是溶液的质量不相同,则析出的晶体质量不一定;故选项错误。
D、20℃时,甲、乙饱和溶液的质量分数相同,将20℃的甲、乙饱和溶液升温至40℃,甲乙的溶解度均增大,但溶质均没有增大,所得溶液的溶质质量分数也不变;故选项错误。
故选:A。

【题目】下面是某化学兴趣小组的同学对氢氧化钠部分性质的探究过程:
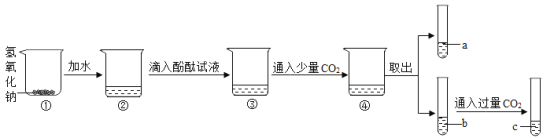
(1)用手触摸②的烧杯外壁,感觉发烫,这是由于氢氧化钠固体溶于水时会_______(填“吸热”或“放热”),③中的溶液显_______色.
(2)从③到④溶液的颜色变化不明显,说明④中的溶液呈______性(填“酸”或“碱”).
(3)c溶液和a溶液对比,c溶液颜色更浅.
(提出问题)为什么继续通入过量的二氧化碳气体溶液颜色会更浅?
(查阅资料)(1)Na2CO3+CO2+H2O==2NaHCO3 (2)Ca(NO3)2溶液与NaHCO3溶液不反应
(设计实验)
实验操作 | 实验现象 | 实验结论 |
取少量c溶液滴入稀盐酸 | ____ | 溶液中含较多的CO32﹣或HCO3﹣ |
另取少量c溶液滴入硝酸钙溶液 | 无明显现象 | 溶液中没有大量的____离子 |
(实验结论)根据甲、乙两个实验得出的结论,写出甲实验中发生反应的化学方程式:_____________________________.
(实验反思)同种反应物在不同的条件下发生化学反应时,可能得到不同的产物.如:碳在氧气中燃烧可以生成________或________.
(实验拓展)106g10% Na2CO3溶液与Ca(NO3)2完全反应生成沉淀 ______g
【题目】推理是学习化学的一种重要方法,但不合理的推理会得出错误的结论.请对下列错误观点用化学式或化学方程式写出相应的否定例证.
错误观点 | 否定例证 | |
① | 有单质和化合物生成的反应一定是置换反应 | 举例:CuO+CO |
② | 均一、稳定的液体一定是溶液 | __ |
③ | 含有碳元素的化合物一定是有机物 | __ |
④ | 生成盐和水的反应一定是中和反应 | __ |