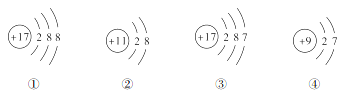题目内容
【题目】鸡量主要由蛋壳、蛋壳膜、蛋白、蛋黄等几个部分组成,其中蛋壳的主要成分是CaCO3,里一层蛋壳膜。化学活动兴趣小组的同学开了以下探究活动:
(提出问题)蛋壳中的 CaCO3含量是多少?
(查阅资料)
a、蛋壳经过科学检测其中含CaCO3的质量分数的为82%~85%,含蛋白质质量分数的14-17%
b、蛋壳膜中蛋白质含量的为90%~93%。
c、Ba(OH)2是一种碱,化学性质与Ca(OH)2相似。
(设计方案)
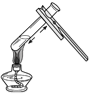
方案一:用“灼烧法”,将该蛋壳放在空气中充分灼烧并采集相关数据进行测定。
方案二:用“酸处理法”,将蛋壳与稀盐酸反应后再进行吸收转变为碳酸钡进行测量处理。
(进行实验)
方案一:称取12.0g蛋壳研磨成粉末置于通风橱中,灼烧至质量不再减少,再称量剩余固体的质量为7.16g
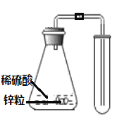
方案二:用图2所示的连接实验装置。称取12g蛋壳样品进行实验(假设其他成分均不与HCI反应,装置内试剂均足量。)
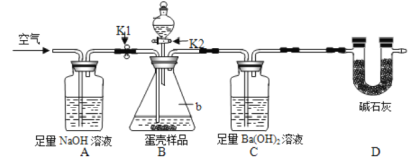
(实验步骤)
①按如图连接好装置后,并____________;
②向B装置中加入蛋壳样品后,先通入一会儿空气;
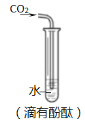
③关闭K1,打开K2,向蛋壳样品中滴入10%的盐酸,直到________为止;
④关闭K2,打开K1,再缓缓通入空气一会儿,至装置C中不再产生沉淀为止;
⑤将装置C中的固液混合物进行过滤、洗涤、烘干后称量其质量;
⑥重复上述实验
(数据处理)
方案一:产生的CO2质量_______g,蛋壳中CaCO3的质量分数为_______。(保留一位小数)
方案二:重复3次实验,记录数据如下:
实验次数 | 第1次 | 第2次 | 第3次 |
装置C中沉淀质量(/g) | 19.68 | 19.75 | 19.67 |
方案二中重复进进行实验的目的__________;生成沉淀的化学方程式是_________。实验测得蛋壳中的CaCO3的质量分数为________。
(评价反思)
(1)方案二中装置D的作用是_________。
(2)方案一测定值与科学检测的数据有较大误差,主要原因是________。
【答案】检查装置气密性 不产生气泡 4.84 91.7% 减小实验误差 Ba(OH)2+CO2=BaCO3↓+H2O 83.3% 防止氢氧化钡吸收空气中的二氧化碳 灼烧时碳酸钙以外的物质反应也能产生气体
【解析】
[实验步骤]①有气体参与的反应,需要检验装置的气密性,所以按如图连接好装置后,并检查装置气密性;
③碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,所以关闭K1,打开K2,向蛋壳样品中滴入10%的盐酸,直到不产生气泡为止;
[数据处理]方案一:碳酸钙在高温的条件下生成氧化钙和二氧化碳,
生成二氧化碳的质量为:12g-7.16g=4.84g
设碳酸钙的质量分数为x
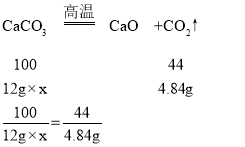
x=91.7%;
方案二:多次测量可以减小实验误差,氢氧化钡和二氧化碳反应生成碳酸钡碳酸钡沉淀和水,所以方案二中重复进进行实验的目的:减小实验误差,生成沉淀的化学方程式是:Ba(OH)2+CO2=BaCO3↓+H2O;
碳酸钡的质量为:![]() =19.7g,
=19.7g,
设参加反应的碳酸钙的质量为x
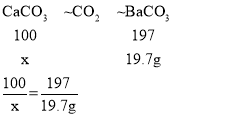
x=10g
所以蛋壳中的CaCO3质量分数为:![]() ×100%=83.3%;
×100%=83.3%;
[评价反思](1)氢氧化钡吸收空气中的二氧化碳,会造成实验误差,所以方案二中装置D的作用是:防止氢氧化钡吸收空气中的二氧化碳;
(2)方案一测定值与科学检测的数据有较大误差,主要原因是:灼烧时碳酸钙以外的物质反应也能产生气体。
故答案为:[实验步骤]①检查装置气密性;
③不产生气泡;
[数据处理]方案一:4.84;91.7%;
方案二:减小实验误差,Ba(OH)2+CO2=BaCO3↓+H2O;83.3%;
[评价反思](1)防止氢氧化钡吸收空气中的二氧化碳;
(2)灼烧时碳酸钙以外的物质反应也能产生气体。

 全优点练单元计划系列答案
全优点练单元计划系列答案【题目】下表实验内容中的横、纵坐标表示的量符合下图所示变化趋势的是
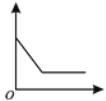
序号 | 实验内容 | 横坐标表示的量 | 纵坐标表示的量 |
① | 盐酸加水稀释 | 加入水的体积 | 溶液的pH |
② | 过量红磷测定空气中氧气含量 | 时 间 | 红磷质量 |
③ | 过氧化氢溶液与二氧化锰制氧气 | 时 间 | 二氧化锰质量 |
④ | 向铜、锌混合物粉末中加入盐酸 | 盐酸质量 | 剩余固体质量 |
A.①②B.①④
C.②③D.②④
【题目】下面是某化学兴趣小组的同学对氢氧化钠部分性质的探究过程:
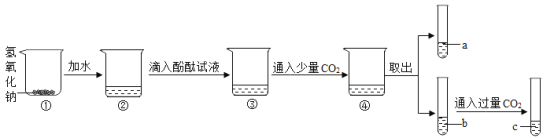
(1)用手触摸②的烧杯外壁,感觉发烫,这是由于氢氧化钠固体溶于水时会_______(填“吸热”或“放热”),③中的溶液显_______色.
(2)从③到④溶液的颜色变化不明显,说明④中的溶液呈______性(填“酸”或“碱”).
(3)c溶液和a溶液对比,c溶液颜色更浅.
(提出问题)为什么继续通入过量的二氧化碳气体溶液颜色会更浅?
(查阅资料)(1)Na2CO3+CO2+H2O==2NaHCO3 (2)Ca(NO3)2溶液与NaHCO3溶液不反应
(设计实验)
实验操作 | 实验现象 | 实验结论 |
取少量c溶液滴入稀盐酸 | ____ | 溶液中含较多的CO32﹣或HCO3﹣ |
另取少量c溶液滴入硝酸钙溶液 | 无明显现象 | 溶液中没有大量的____离子 |
(实验结论)根据甲、乙两个实验得出的结论,写出甲实验中发生反应的化学方程式:_____________________________.
(实验反思)同种反应物在不同的条件下发生化学反应时,可能得到不同的产物.如:碳在氧气中燃烧可以生成________或________.
(实验拓展)106g10% Na2CO3溶液与Ca(NO3)2完全反应生成沉淀 ______g