题目内容
【题目】甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。下列说法正确的是( )

A. t1℃时,甲、乙两物质的饱和溶液中溶质的质量分数相等,且都等于 60%
B. t2℃时,甲、乙两种物质的饱和溶液,降温至t1℃,析出晶体质量,甲不一定大于乙
C. t1℃时,将甲、乙两种物质的饱和溶液升温至t2℃时,溶质的质量分数甲大于乙
D. t1℃时,将甲、乙两种物质的饱和溶液分别降温到0℃,乙析出晶 体比甲析出晶体多
【答案】B
【解析】
A、由溶解度曲线可知,t1℃时,甲、乙两物质的溶解度相等为60g。故t1℃时,甲、乙两物质的饱和溶液中溶质的质量分数相等,且都等于![]() ×100%= 37.5%,选项错误;
×100%= 37.5%,选项错误;
B、由于甲、乙两种物质的饱和溶液的质量不确定,故t2℃时,甲、乙两种物质的饱和溶液,降温至t1℃,析出晶体质量,甲不一定大于乙,选项正确;
C、由溶解度曲线可知,t1℃时,甲、乙两物质的溶解度相等,溶质质量分数相等,溶解度随温度的升高而增大。由t1℃升温至t2℃时,温度升高,甲、乙两种溶液中溶质、溶剂质量不变,故溶质质量分数不变,选项错误;
D、由于甲、乙两种物质的饱和溶液的质量不确定,故t1℃时,将甲、乙两种物质的饱和溶液分别降温到0℃,甲、乙析出晶体的质量无法比较,选项错误。故选B。

 心算口算巧算一课一练系列答案
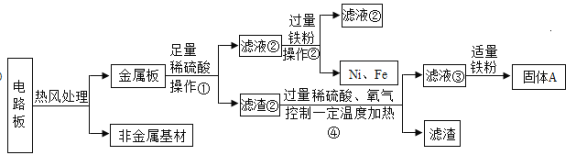
心算口算巧算一课一练系列答案【题目】小明同学家新换了水龙头,从说明书上了解到该水龙头是钢质镀铬。好奇的小明想探究铬(Cr)与常见金属铁、铜的活动性强弱,遨请你一同参加。
(1)作出猜想:
猜想1:Cr>Fe>Cu
猜想2:Fe>Cu>Cr
猜想3:你的猜想是___。
[查阅资料]
①铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
(2)设计实验
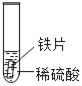
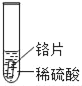
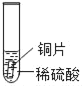
小明同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸。
实验 | 试管1 | 试管2 | 试管3 |
实验操作 |
|
|
|
实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | ___ |
(3)结论与解释:
①小明得到的结论是猜想___正确。
②实验前用砂纸打磨金属片的目的是___。
(4)反思:小明将铬片投入FeSO4溶液中,现象是___,请你写出反应的化学方程式___。
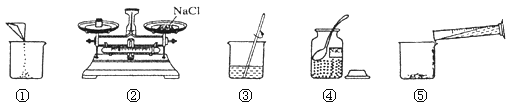
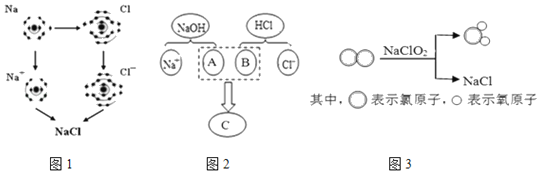
【题目】化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图).经了解得知该无色溶液原存放在盐溶液的柜子里,由此猜测可能是_____,
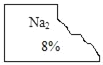
他们提出可能是碳酸钠、碳酸氢钠、硫酸钠 氯化钠、硝酸钠溶液中的一种,于是决定对这瓶溶液进行实验探究。
(理论分析)为了确定该溶液,他首先进行了分析,小组同学根据标签残留部分认为一定不是_____,他们的依据是_____。
(查阅资料)
Na2CO3+HCl=NaCl+NaHCO3 Na2CO3+2HCl=2NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑ Na2CO3+BaCl2=BaCO3↓+2NaCl
(活动探究)
为确定其成分,小新同学设计如下方案进行探究(探究1)
实验步骤 | 现象 | 结论 |
该溶液少许于试管中,滴加过量的BaCl2溶液,振荡 | ①_____ | 则该溶液是Na2SO4溶液 |
过滤,向滤渣滴加稀盐酸 | ②_____ |
(2)小芳认为可以设计更简单的实验方案(探究2)
实验步骤 | 现象 | 结论 |
取该无色溶液少许于试管中,慢慢滴加少量的盐酸 | 没有气泡产生 | 溶液中没有碳酸钠,则该溶液是Na2SO4溶液 |
(解释)你认为上面两位同学对实验结果判定是否正确?请说明理由_____。
(实验反思)在区别判断物质成分时,除考虑物质本身的性质外,还需考虑_____。