题目内容
【题目】为了测定实验中氯酸钾样品的纯度,某兴趣小组取2.5克样品与0.8克二氧化锰混合。加热该混合物t1时间后(假设杂质不参加反应),冷却,称量剩余固体质量,重复以下操作,依次称得加热t1、t2、 t3、t4时间后剩余固体的质量,记录数据如表:
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量/g | 2.48 | 2.41 | 2.34 | 2.34 |
请仔细分析实验数据,回答下列问题:
(1)在多长时间后,该样品中的氯酸钾已经反应完全。
(2)计算完全反应后生成氧气的质量为多少。
(3)求该样品中氯酸钾的质量分数。
【答案】(1)t3 ;(2)0.96g;(3)98%
【解析】
(1)由表中信息可知,t3以后剩余固体质量不再减少,说明氯酸钾已经完全反应。
(2)加热混合物前后,物质的质量差即为反应生成氧气的质量;故生成氧气的质量为:2.5g+0.8g-2.34g=0.96g;
设氯酸钾的质量为![]() ,
,
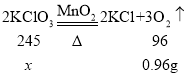
![]()
![]() =2.45g
=2.45g
样品中氯酸钾的质量分数为:![]() ×100%=98%
×100%=98%

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案【题目】铜粉中混有少量的铁粉,为了除去铁粉,某校兴趣小组同学,取该铜粉20g于烧杯中,然后等量分5次加入未知质量分数的某强酸(W)溶液,充分反应后所得数据如下表,请根据相关知识和图表信息回答下列问题。
项目 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
加入W溶液的质量/g | 5 | 5 | 5 | 5 | 5 |
每次产生气体的质量/g | 0.01 | 0.01 | 0.01 | 0.005 | 0 |
(1)写出你所选择酸(W)的化学式 。
(2)铜粉中混有铁粉的质量是 。
(3)计算你选择酸(W)的质量分数(写出计算过程)。
【题目】宜城葛洲坝水泥厂生产的水泥畅销各地,生产的原料之一是石灰石。某化学兴趣小组对石灰石纯度进行探究。取该石灰石样品16g,把200g稀盐酸分四次加入,测量探究过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水也不与稀盐酸反应)。请计算:
序号 | 加入稀盐酸的质量/g | 剩余固体质量/g |
第1次 | 50 | 11 |
第2次 | 50 | 6 |
第3次 | 50 | 3.2 |
第4次 | 50 | m |
(1)表中m的数值为 ;石灰石纯度是 。
(2)求第2次反应完毕后所得溶液溶质的质量分数(写出解题过程,结果精确到0.1﹪)