题目内容
某化工厂生产过程中的残液含有硝酸银,取少量该残液样品,分别盛在A、B两支试管中,再分别加入不同质量的黄铜片(铜锌合金),充分反应后过滤,分别取滤渣和滤液进行下表所示实验.请你参与实验探究:
(1)用化学式填写下列实验报告中的空格:
(2)若要验证B试管得到的滤液中可能含有的溶质,可以采用的物理方法是 ;可以采用的化学方法是向滤液中加入 (填写一种物质的化学式),并观察现象.
(1)用化学式填写下列实验报告中的空格:
| 实验操作 | 实验现象 | 分析与结论 |
| ①将A试管滤出的滤渣洗涤后,取样,再加入稀盐酸 | 有无色气泡产生 | 从A试管得到的滤渣的成分是 |
| ②取少量B试管得到的滤液,滴加少量稀盐酸 | 无明显现象 | 从B试管得到的滤液中的溶质一定有 |
考点:金属活动性顺序及其应用,酸的化学性质
专题:科学探究
分析:在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.锌能与硝酸银反应生成硝酸锌和银,铜能与硝酸银反应生成硝酸铜和银,盐酸能与硝酸银反应生成白色沉淀,硝酸铜能与氢氧化钠反应生成蓝色沉淀.据此分析回答有关的问题.
解答:解:三种金属锌、铜、银的金属活泼性顺序是锌>铜>银,向硝酸银的溶液中加入黄铜,锌先与硝酸银反应,等硝酸银完全反应后,铜与硝酸银反应.充分反应后过滤,分别取滤渣工滤液进行下表所示实验.
(1)①将A试管滤出的滤渣洗涤后加入到稀盐酸中,有气泡产生,说明锌粉过量,硝酸银完全与锌反应,铜没有参加反应,则可知滤渣中含有银、铜和锌;
②向B试管得到的滤液中滴加少量稀盐酸,无明显现象,说明溶液中不含有硝酸银,则说明溶液中一定有硝酸锌,可能含有硝酸铜.故表格空格为:
(2)若要验证B试管得到的滤液中可能含有的溶质.由于硝酸铜溶液显蓝色,可以采用的物理方法是观察溶液的颜色.若溶液显蓝色则含有硝酸铜,显无色,则溶液中不含有硝酸铜;由于硝酸铜能与氢氧化钠反应生成蓝色沉淀可以采用的化学方法是向滤液中加入NaOH,并观察现象.
故答为:(1)见上表;(2)观察溶液的颜色,NaOH.
(1)①将A试管滤出的滤渣洗涤后加入到稀盐酸中,有气泡产生,说明锌粉过量,硝酸银完全与锌反应,铜没有参加反应,则可知滤渣中含有银、铜和锌;
②向B试管得到的滤液中滴加少量稀盐酸,无明显现象,说明溶液中不含有硝酸银,则说明溶液中一定有硝酸锌,可能含有硝酸铜.故表格空格为:
| 实验操作 | 实验现象 | 分析与结论 |
| ①将A试管滤出的滤渣洗涤后,取样,再加入稀盐酸 | 有无色气泡产生 | 从A试管得到的滤渣的成分是银、铜和锌 |
| ②取少量B试管得到的滤液,滴加少量稀盐酸 | 无明显现象 | 从B试管得到的滤液中的溶质一定有 硝酸锌,可能有硝酸铜. |
故答为:(1)见上表;(2)观察溶液的颜色,NaOH.
点评:本题考查了金属活动性顺序的应用常见离子的颜色检验等知识,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
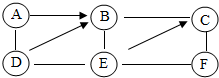 已知A-F均为初中化学中常见的物质,B是最常见的金属,且与C溶液反应生成紫红色固体,D是红粽色金属氧化物,E含有三种元素,其稀溶液常用于除铁锈,F是一种常见的碱,它们之间存在如图所示的转化关系(反应条件即部分生成物省略).
已知A-F均为初中化学中常见的物质,B是最常见的金属,且与C溶液反应生成紫红色固体,D是红粽色金属氧化物,E含有三种元素,其稀溶液常用于除铁锈,F是一种常见的碱,它们之间存在如图所示的转化关系(反应条件即部分生成物省略).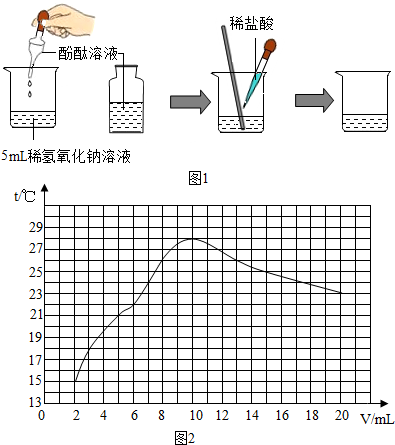
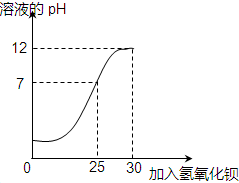 取某稀硫酸溶液22.33g,逐滴加入30g某未知浓度的氢氧化钡溶液,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示).过滤后得滤液50g,请计算该滤液中溶质的质量分数(计算结果精确到0.001%).
取某稀硫酸溶液22.33g,逐滴加入30g某未知浓度的氢氧化钡溶液,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示).过滤后得滤液50g,请计算该滤液中溶质的质量分数(计算结果精确到0.001%).