题目内容
【题目】酸、碱、盐是九年级化学学习的重要知识,它们具有广泛的用途。
(1)酸、碱、盐之间的反应中,生成物中一定有_____生成。
A 水 B 盐 C 沉淀 D 气体
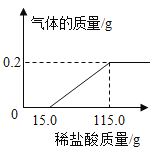
(2)向硝酸银、硝酸铜和硝酸镁的混合溶液中逐渐加入锌粉,溶液质量与加入锌的质量关系如图1所示。
①写出b点时溶液中溶质的化学式_____。
②经测定a点和c点时溶液的质量相等,请分析原因_____。
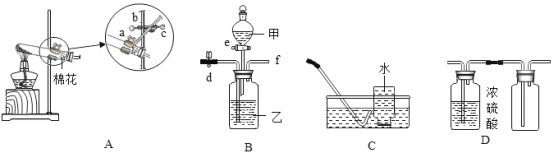
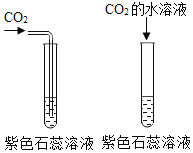
(3)某化学小组选用稀盐酸和石灰石用如图2所示装置制备干燥的CO2,并检验其性质。
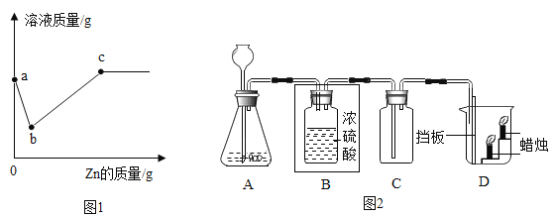
①请把B装置中的导管补画完整。_____
②请写出用C装置收集CO2的原因_____。
③根据D中的现象写出一个CO2的用途_____。
④某同学想用A装置制取氧气,请写出该反应的方程式_____。
⑤若50g稀盐酸与含5.0g碳酸钙的石灰石恰好完全反应(杂质不参与反应),则该稀盐酸的溶质质量分数为多少_____?
【答案】B Zn(NO3)2、Cu(NO3)2、Mg(NO3)2 根据金属置换规律可知,锌能和硝酸银溶液、硝酸铜溶液反应,化学方程式为:Zn+2AgNO3=Zn(NO3)2+2Ag、Zn+Cu(NO3)2=Zn(NO3)2+Cu,由化学方程式可知,每65份质量的锌置换出来216份质量的银,使溶液的质量减少;每65份质量的锌置换出来64份质量的铜,使溶液质量增加,当到c点时,锌置换银使溶液减少的质量正好等于锌置换铜使溶液增加的质量  二氧化碳的密度比空气大 可用于灭火 2H2O2
二氧化碳的密度比空气大 可用于灭火 2H2O2![]() 2H2O+O2↑ 7.3%
2H2O+O2↑ 7.3%
【解析】
(1)酸和碱反应生成盐和水;酸和盐反应生成新酸和新盐;碱和盐反应生成新碱和新盐,所以酸、碱、盐之间的反应中,生成物中一定有盐生成,故选B;
(2)①向硝酸银、硝酸铜和硝酸镁的混合溶液中逐渐加入锌粉,根据金属置换规律可知,锌先硝酸银反应,然后再和硝酸铜反应,锌不和硝酸镁反应,b点表示锌和硝酸银恰好完全反应,锌和硝酸银反应生成硝酸锌和银,溶液中的溶质有:硝酸锌、硝酸铜和硝酸镁;
②根据金属置换规律可知,锌能和硝酸银溶液、硝酸铜溶液反应,化学方程式为:Zn+2AgNO3=Zn(NO3)2+2Ag、Zn+Cu(NO3)2=Zn(NO3)2+Cu,由化学方程式可知,每65份质量的锌置换出来216份质量的银,使溶液的质量减少;每65份质量的锌置换出来64份质量的铜,使溶液质量增加,当到c点时,锌置换银使溶液减少的质量正好等于锌置换铜使溶液增加的质量;
(3)①二氧化碳不和浓硫酸反应,要想用浓硫酸干燥二氧化碳就要让二氧化碳和浓硫酸接触,所以把B装置中的导管补画完整后的图如右图所示: ;
;
②因为二氧化碳的密度比空气大,所以能用向上排空气法收集;
③由D中的现象可知二氧化碳不燃烧也不支持燃烧,因此二氧化碳可用于灭火;
④A装置不能加热,适合于过氧化氢分解制取氧气,化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
⑤设5.0g碳酸钙完全反应需要HCl的质量为x
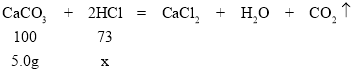
![]()
x=3.65g
该稀盐酸的溶质质量分数为:
![]() =7.3%
=7.3%
答:该稀盐酸的溶质质量分数为7.3%。

 阅读快车系列答案
阅读快车系列答案