题目内容
A~F分别是氢气、氧气、氮气、一氧化碳、二氧化碳、甲烷六种气体中的一种.A是最理想的清洁燃料;C与D在B中燃烧均有F生成,其中C中两种元素的质量比为3:1,请回答下列问题.
(1)D为 ;E为 .
(2)C与B反应的化学方程式为 ;
(3)请写出B的一条用途 .
(1)D为
(2)C与B反应的化学方程式为
(3)请写出B的一条用途
分析:根据题意,A~F分别是氢气、氧气、氮气、一氧化碳、二氧化碳、甲烷六种气体中的一种,A是最理想的清洁燃料,因此A是氢气;C与D在B中燃烧均有F生成,可推出B为氧气,又C中两种元素的质量比为3:1,可以推出为C甲烷,F为二氧化碳,D为一氧化碳,剩余的气体E为氮气,据此分析.
解答:解;A~F分别是氢气、氧气、氮气、一氧化碳、二氧化碳、甲烷六种气体中的一种,A是最理想的清洁燃料,因此A是氢气;C与D在B中燃烧均有F生成,可推出B为氧气,又C中两种元素的质量比为3:1,可以推出为C甲烷,F为二氧化碳,D为一氧化碳,剩余的气体E为氮气,因此:
(1)D为一氧化碳,E为氮气;
(2)C与B反应是甲烷和氧气生成二氧化碳和水,反应的方程式为:CH4+2O2
2H2O+CO2;
(3)氧气可以供给生物呼吸或医疗急救等等(其他合理答案均可).
故答案为:(1)D:一氧化碳(CO);E:氮气(N2)
(2)CH4+2O2
2H2O+CO2
(3)供给生物呼吸或医疗急救等等(其他合理答案均可).
(1)D为一氧化碳,E为氮气;
(2)C与B反应是甲烷和氧气生成二氧化碳和水,反应的方程式为:CH4+2O2
| ||
(3)氧气可以供给生物呼吸或医疗急救等等(其他合理答案均可).
故答案为:(1)D:一氧化碳(CO);E:氮气(N2)
(2)CH4+2O2
| ||
(3)供给生物呼吸或医疗急救等等(其他合理答案均可).
点评:要想解答好本题,就要掌握氧气、氢气、一氧化碳、二氧化碳、甲烷的不同性质,根据燃烧的产物区别三种可燃性气体:甲烷燃烧生成二氧化碳和水,氢气燃烧只生成水,一氧化碳燃烧只生成二氧化碳.

练习册系列答案
相关题目
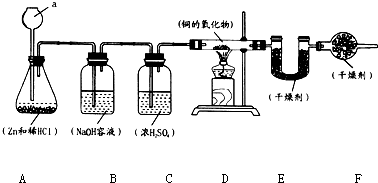 实验室用锌和稀盐酸制取氢气,并用氢气还原铜的一种氧化物的实验来测定该氧化物的组成.实验装置如图所示:
实验室用锌和稀盐酸制取氢气,并用氢气还原铜的一种氧化物的实验来测定该氧化物的组成.实验装置如图所示:

 实验室用锌和稀盐酸制取氢气,并用氢气还原铜的一种氧化物的实验来测定该氧化物的组成.实验装置如图所示:
实验室用锌和稀盐酸制取氢气,并用氢气还原铜的一种氧化物的实验来测定该氧化物的组成.实验装置如图所示: