题目内容
实验室用锌和稀盐酸制取氢气,并用氢气还原铜的一种氧化物的实验来测定该氧化物的组成.实验装置如图所示:试回答下列问题:
(1)仪器a的名称是______,a仪器下端管口插入液面下的目的是______.
(2)B、C、F装置的作用分别是:B______,C______,F______.
(3)在点燃D装置中酒精灯以前,要将氢气通过整个装置一段时间的目的是______.
(4)A中产生的现象是______,反应的化学方程式是______.
(5)已知D装置中铜的氧化物的质量为7.2g,当其完全被还原时,称得E装置增重0.9g,则这种铜的氧化物中铜元素和氧元素的质量比的原始计算式为______,其化学式为______.
(6)如果B、C装置的顺序颠倒,将造成铜、氧两元素的质量之偏______(填“高”或“低”),原因是______.

【答案】分析:根据已有的知识进行分析,使用氢气进行实验时,必须是纯净的氢气,需要除去氢气中混有的水蒸气和氯化氢气体,具有可燃性的气体不纯时加热或点燃可能产生爆炸,根据题干提供的数据,结合物质间的反应即可写出计算式.
解答:解:(1)据图可知,a是长颈漏斗,长颈漏斗末端浸没到液面以下能防止生成的氢气从长颈漏斗逸出,故填:长颈漏斗;防止生成的氢气从长颈漏斗口逸出;
(2)氢氧化钠溶液能除去氢气中混有的氯化氢气体,浓硫酸具有吸水性,能除去氢气中的水蒸气,F中的干燥剂能防止空气中的水蒸气进入E装置,故填:除去氢气中的氯化氢气体;除去氢气中的水蒸气;吸收空气中的水蒸气,防止进入E装置;
(3)氢气具有可燃性,不纯时加热易产生爆炸,需要先通入一段时间氢气,以把装置中的空气排尽,故填:排除整个装置内的空气,防止加热时发生爆炸;
(4)锌能与稀盐酸反应生成氢气,同时生成易溶于水的氯化锌,故会观察到有大量的气泡产生,且锌粒逐渐溶解,故填:产生大量气泡,锌粒逐渐溶解;Zn+2HCl=ZnCl2+H2↑;
(5)E装置增重0.9g,说明生成水的质量为0.9g,水中含有的氧元素的质量就是铜的氧化物中含有的氧元素的质量,氧元素的质量为: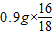 ,铜元素的质量为:
,铜元素的质量为: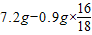 ,故铜元素和氧元素的质量比的算式为:
,故铜元素和氧元素的质量比的算式为: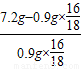 ,铜元素的质量为6.4g,氧元素的质量为0.8g,则在该铜的氧化物中铜氧原子的个数比为:
,铜元素的质量为6.4g,氧元素的质量为0.8g,则在该铜的氧化物中铜氧原子的个数比为: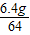 :
: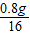 =2:1,故该铜的氧化物为Cu2O,故填:
=2:1,故该铜的氧化物为Cu2O,故填: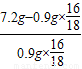 ;Cu2O;
;Cu2O;
(6)若氢氧化钠溶液和浓硫酸交换位置,则会使水蒸气进入E装置,导致测得的水的质量增多,从而氧元素的质量偏大,导致铜元素的质量偏小,最终算得的铜氧元素的质量偏低,故填:低;B装置中的水蒸气会随气流进入E装置,使测出水的质量增加,从而导致由水计算出的氧元素的质量增大,铜元素质量减少,最终导致结果偏低.
点评:本题考查了物质中元素含量的测定,完成此题,可以依据实验提供的数据结合物质的性质进行.
解答:解:(1)据图可知,a是长颈漏斗,长颈漏斗末端浸没到液面以下能防止生成的氢气从长颈漏斗逸出,故填:长颈漏斗;防止生成的氢气从长颈漏斗口逸出;
(2)氢氧化钠溶液能除去氢气中混有的氯化氢气体,浓硫酸具有吸水性,能除去氢气中的水蒸气,F中的干燥剂能防止空气中的水蒸气进入E装置,故填:除去氢气中的氯化氢气体;除去氢气中的水蒸气;吸收空气中的水蒸气,防止进入E装置;
(3)氢气具有可燃性,不纯时加热易产生爆炸,需要先通入一段时间氢气,以把装置中的空气排尽,故填:排除整个装置内的空气,防止加热时发生爆炸;
(4)锌能与稀盐酸反应生成氢气,同时生成易溶于水的氯化锌,故会观察到有大量的气泡产生,且锌粒逐渐溶解,故填:产生大量气泡,锌粒逐渐溶解;Zn+2HCl=ZnCl2+H2↑;
(5)E装置增重0.9g,说明生成水的质量为0.9g,水中含有的氧元素的质量就是铜的氧化物中含有的氧元素的质量,氧元素的质量为:
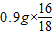 ,铜元素的质量为:
,铜元素的质量为: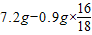 ,故铜元素和氧元素的质量比的算式为:
,故铜元素和氧元素的质量比的算式为: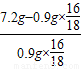 ,铜元素的质量为6.4g,氧元素的质量为0.8g,则在该铜的氧化物中铜氧原子的个数比为:
,铜元素的质量为6.4g,氧元素的质量为0.8g,则在该铜的氧化物中铜氧原子的个数比为: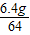 :
: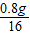 =2:1,故该铜的氧化物为Cu2O,故填:
=2:1,故该铜的氧化物为Cu2O,故填: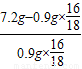 ;Cu2O;
;Cu2O;(6)若氢氧化钠溶液和浓硫酸交换位置,则会使水蒸气进入E装置,导致测得的水的质量增多,从而氧元素的质量偏大,导致铜元素的质量偏小,最终算得的铜氧元素的质量偏低,故填:低;B装置中的水蒸气会随气流进入E装置,使测出水的质量增加,从而导致由水计算出的氧元素的质量增大,铜元素质量减少,最终导致结果偏低.
点评:本题考查了物质中元素含量的测定,完成此题,可以依据实验提供的数据结合物质的性质进行.

练习册系列答案
相关题目

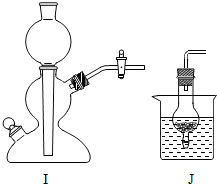
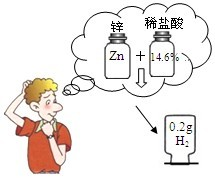 右图所示为某同学在实验室用锌和稀盐酸制取并临时存放氢气.请根据要求回答问题:
右图所示为某同学在实验室用锌和稀盐酸制取并临时存放氢气.请根据要求回答问题:
