题目内容
【题目】气体制取是重要的化学实验活动。
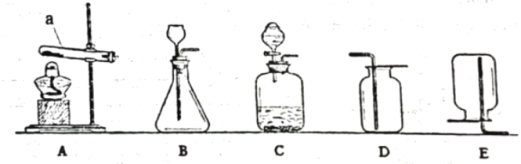
①仪器a的名称是________。
②实验室制取二氧化碳可选择的装置组合是_______。
③用双氧水和二氧化锰制取氧气的化学方程式为_________ ;相对于装置B,装置C的优点是___ 。
④实验室常用氯酸钾和二氧化锰制取氧气,向试管中加入药品的正确操作是_________。
I.先加氯酸钾,后加二氧化锰
II.先加二氧化锰,后加氯酸钾
Ⅲ.加入混合好的氯酸钾和二氧化锰
⑤能收集氧气的装置是_________。
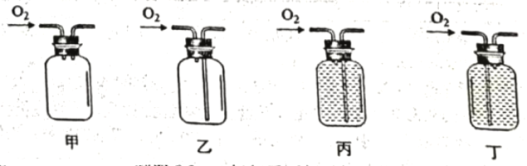
⑥根据化学方程式列式计算,制取0.3mol氧气需要氯酸钾的物质的量是多少_______?
【答案】试管 BD或CD 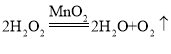 可以控制滴加液体的速率,使反应平稳进行,得到较平稳的气流 III 丙 0.2mol
可以控制滴加液体的速率,使反应平稳进行,得到较平稳的气流 III 丙 0.2mol
【解析】
①、a为用于加热的试管;
故答案为:试管。
②、制取二氧化碳为固液不加热装置,所以可以选择B或C装置为发生装置,二氧化碳密度比空气大,所以可以选择向上排空法收集气体,因此收集装置为D;
故答案为:BD或CD。
③、过氧化氢在二氧化锰催化作用下分解生成水和氧气,据此书写化学方程式;装置C带有开关,可以控制加入液体的量,从而控制液体加入速率,保证反应平稳进行,得到较平稳的气流;
故答案为: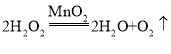 ;可以控制滴加液体的速率,使反应平稳进行,得到较平稳的气流。
;可以控制滴加液体的速率,使反应平稳进行,得到较平稳的气流。
④、由于二氧化锰作为催化剂使用,所以需要充分与氯酸钾接触,因此需要将两者混合均匀后,再装入试管加热;
故答案为:Ⅲ。
⑤、氧气密度比空气大,所以进入集气瓶先在底部聚集,因此从长管进气,短管排气,达到收集气体的目的,所以甲乙错误;氧气不易溶于水,且密度比水小,所以现在上部聚集,因此从短口进气,长口排出水,达到收集氧气的目的,所以选择丙进行收集;
故答案为:丙。
⑥、设需要氯酸钾的物质的量为n,
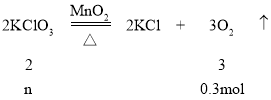
![]()
n=0.2mol;
故答案为:0.2mol。

 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案【题目】了解日用化工品的成分,有利于我们正确使用。
名称 | 洗洁精 | 炉具清洁剂 | 洁厕灵 | “84”消毒液 |
有效成分 | 表面活性剂 | 氢氧化钠 | 盐酸 | 次氯酸钠 |
(1)洗洁精能清洗餐具上的油污,是因为它具有______功能。
(2)炉具清洁剂的pH___7(填“>”“<”“或“=”)。使用时禁止与皮肤接触是因为氢氧化钠___性.
(3)不能用洁厕灵清洗铁制品的原因是______(用化学方程式表示)。
(4)洁厕灵与“84”消毒液不能混合使用,因为两者混合会发生反应:![]() ,生成的气体X有毒。X的化学式为____。
,生成的气体X有毒。X的化学式为____。
【题目】氢化钙(CaH2)是一种白色细颗粒状固体,能与水发生剧烈反应,其反应的化学方程式为:![]() ,常用作登山运动员的能源提供剂。某化学实验小组为了探究氢化钙的性质,将一定量的CaH2加入到碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。充分反应后过滤,得到滤渣和滤液,滤渣的主要成分是_____。为进一步确定滤液中所含溶质的成分,他们进行了以下实验探究。
,常用作登山运动员的能源提供剂。某化学实验小组为了探究氢化钙的性质,将一定量的CaH2加入到碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。充分反应后过滤,得到滤渣和滤液,滤渣的主要成分是_____。为进一步确定滤液中所含溶质的成分,他们进行了以下实验探究。
[提出猜想]猜想一: NaOH
猜想二: NaOH 和Ca(OH)2
猜想三: NaOH、Na2CO3
猜想四: NaOH、 Na2CO3、 Ca(OH)2
经过讨论,大家一致认为猜想四不合理,理由是(用化学方程式表示)______。
[实验验证]
实验 | 现象 | 结论 |
(1)取少量滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想___不成立 |
(2)另取少量滤液,向其中加入______ | _____ | 猜想三成立 |
[反思与拓展]若向NH4Cl的溶液中加入一定量的CaH2,充分反应,产生的气体有氢气和___。