题目内容
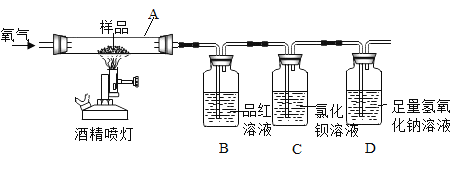
【题目】我国一些城市使用焦炉煤气作为生活燃料。以下实验流程是对焦炉煤气的成分进行局部 探究。下列说法不正确的是
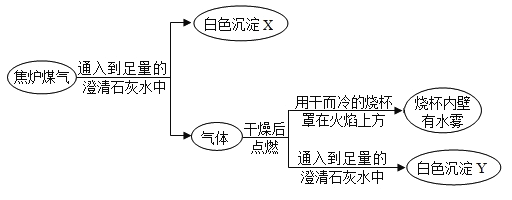
A.焦炉煤气可能含有 COB.X、Y 都是碳酸钙
C.上述流程中可能有化合反应发生D.焦炉煤气中一定含有 CO2 和 CH4
【答案】D
【解析】
A、焦炉煤气点燃后产生二氧化碳,通入澄清的石灰水变浑浊,则可能含有 CO;故选项正确,但不符合题意;
B、焦炉煤直接气通入澄清的石灰水变浑浊,则白色沉淀X是碳酸钙,焦炉煤气点燃后产生二氧化碳,通入澄清的石灰水变浑浊,则白色沉淀Y 是碳酸钙;故选项正确,但不符合题意;
C、上述流程中干燥后的气体点燃,产生水雾,可能是混合物气体中,氢气在氧气中燃烧生成水,该反应符合“多变一”,可能有化合反应发生;故选项正确,但不符合题意;
D、焦炉煤气中一定含有 CO2 、可能有甲烷、氢气、一氧化碳等气体;故选项错误,但符合题意;
故选:D。

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案【题目】小红按下图装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体。
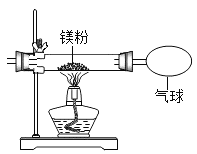
(提出问题)黄色固体是什么?
(查阅资料)①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
(作出猜想)黄色固体是Mg3N2。
(实验探究)设计实验,验证猜想:
实验操作 | 实验现象及结论 |
__________ | ___________ |
(反思与交流)①空气中N2的含量远大于O2的含量,可是镁条在空气中的燃烧产物MgO却远多于Mg3N2,合理的解释是________。
②同学们又联想到氢气在氯气中能够燃烧,于是对燃烧条件又有了新的认识________。
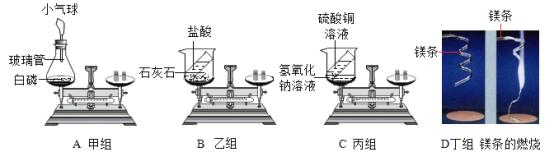
【题目】九年级课外活动小组的同学们在期末复习时,来到化学实验室亲自对“质量守恒定律”进行了再次探究,如图是他们根据这一学期学过的化学反应分别设计的实验,请你一起参与他们的探究活动,并回答相关问题
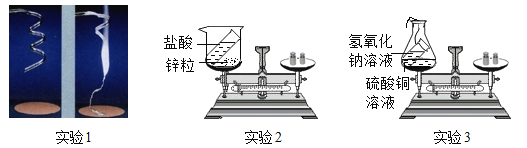
实验1:称量镁条,点燃,待反应结束后,再称量。
实验2:将盛有稀盐酸的小试管放入盛有锌粒的烧杯中称量,然后使稀盐酸与锌粒接触,充分反应后再称量实验3:将盛有氢氧化钠溶液的小试管放入盛有硫酸铜溶液的锥形瓶中称量,然后使氢氧化钠溶液与硫酸铜溶液混合,充分反应后再称量。
编号 | 实验1 | 实验2 | 实验3 |
反应前称重质量 | 9.6g | 212.6g | 118.4g |
反应后称重质量 | 16.0g | 212.4g | 118.4g |
(1)实验1观察到的现象是_______________;
(2)写出实验3反应的化学方程式________________;
(3)上述三个反应______________(填“符合”或“不符合”)质量守恒定律,实验___________正确反映了反应物与生成物的质量关系;
(4)由上述实验我们得到启示,探究_______________的反应验证质量守恒定律,实验必须在密闭的装置中进行;
(5)由质量守恒定律可知,化学反应前后,一定不变的是 _____________(填序号);
①物质种类 ②元素种类 ③原子种类 ④分子种类 ⑤分子数目 ⑥原子数目