题目内容
【题目】自来水消毒过程中通常会发生如下化学反应,其反应的微观过程可用如图表示:
(![]() 表示氯原子,
表示氯原子,![]() 表示氧原子,
表示氧原子,![]() 表示氢原子)
表示氢原子)
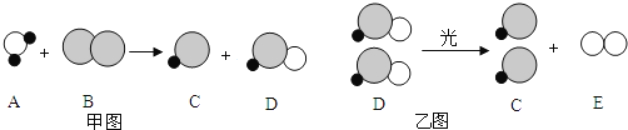
(1)请写出甲图所示反应的化学方程式_____;
(2)乙图所示反应的基本反应类型为_____;
(3)上述物质中,属于单质的有_____(填化学式);
(4)以甲图为例分析,你能总结出的一条结论是_____。
【答案】H2O+Cl2═HCl+HClO; 分解反应; Cl2、O2; 化学反应前后原子的种类、数目不变。
【解析】
(1)通过反应的模型图及物质的微观构成模型图可知:反应物是氯气和水,生成物是盐酸和次氯酸,各物质的微粒个数关系是1:1:1:1,反应的方程式为:Cl2+H2O═HCl+HClO;
(2)由乙图模型图及物质的微观构成模型图可以看出:反应物是一种,生成物是两种,属于分解反应;
(3)单质的分子中含有一种原子,所以可知甲、乙反应中涉及到到的单质有氯气、氧气,化学式为:Cl2,O2;
(4)从甲图可以看出:反应前有一个氧原子、两个氢原子、两个氯原子,反应后也有一个氧原子、两个氢原子、两个氯原子,反应前后原子的种类和数目没有改变。

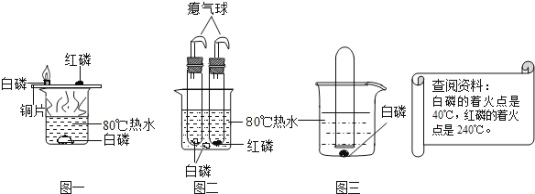
【题目】铁与水蒸气在高温条件下反应生成一种铁的氧化物和一种气体单质,实验装置如图所示。

(1)试管尾部放一团湿棉花的目的是_____。
(2)用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到上方空中,说明生成的气体是_____。
(3)探究试管中剩余固体成分。
(查阅资料)①几种常见铁的氧化物的颜色、状态及能否被磁铁吸引如下表所示。
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
②四氧化三铁能与稀硫酸反应:Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O
(初步实验验证)试管中剩余固体为黑色,能全部被磁铁吸引,则剩余固体一定不含的铁的氧化物是_____、_____ 。
(猜想与假设)猜想一:剩余固体是Fe3O4;猜想二:剩余固体是_____ 。
(继续进行实验)
实验操作 | 实验现象 | 实验结论 |
取少量黑色固体于试管中,滴加足量的稀硫酸。 | _____ | 猜想二成立。 |
(实验结论)铁和水蒸气反应的化学方程式为_____。
【题目】为了探究石灰石的纯度(假设样品中的杂质既不溶于水也不与盐酸反应),兴趣小组进行如下实验:先称取40g石灰石样品均分为4等份分别加入到四个烧杯中,然后再分别加入一定质量的相同浓度的盐酸,实验数据如表所示:
实验编号 | ① | ② | ③ | ④ |
稀盐酸的质量/g | 25 | 50 | 75 | 100 |
剩余固体的质量/g | 7.5 | 5 | 3 | 3 |
(1)石灰石的纯度是_____;
(2)计算所用稀盐酸的溶质质量分数_____(写出计算过程);
(3)实验④所得溶液中溶质的成分是_____(填写化学式)。
【题目】根据下列装置图,回答有关问题:

(1)实验室里制取气体时,根据_____、反应条件确定气体发生装置。完成下表:
气体 | 气体发生装置 | 化学方程式 |
氧气 | A | _____。 |
二氧化碳 | B | _____。 |
(2)十八世纪,瑞典化学家舍勒用如图装置制备氧气,曲颈甑中装有硝酸钾与浓硫酸的混合物,置于火炉上加热,产生的氧气用动物膀胱做成的口袋收集。若改用上图中的发生装置进行该实验,最合适的是_____(填字母)。

(3)实验室里用锌粒与稀硫酸反应制取氢气,以装置B作为发生装置,长颈漏斗的下端必须_____;以装置D作为发生装置,用分液漏斗添加稀硫酸的优点是_____,分液漏斗可以用_____替换。
(4)一定质量的锌粒与98g质量分数为10%的稀硫酸恰好完全反应,最多生成氢气的质量是多少_____?最后所得溶液的溶质质量分数是多少?_____(写出计算过程)