题目内容
【题目】下列各组物质的溶液不用其他试剂就可鉴别的是( )
A. HCl、![]() 、
、![]() 、
、![]() B.
B. ![]() 、
、![]() 、HCl、
、HCl、![]()
C. ![]() 、
、![]() 、
、![]() 、NaOHD.
、NaOHD. ![]() 、
、![]() 、HCl、
、HCl、![]()
【答案】C
【解析】
A、CuCl2溶液是蓝色的,首先鉴别出蓝色的CuCl2溶液,但其余两两混合均没有明显现象,故不加其它试剂无法鉴别;
B、Na2CO3、(NH4)2CO3均能与稀盐酸反应生成二氧化碳气体,与氯化钡反应均生成碳酸钡白色沉淀,无法鉴别Na2CO3、(NH4)2CO3,故不加其它试剂无法鉴别;
C、FeCl3溶液是黄色的,能与FeCl3溶液反应产生红褐色沉淀的是NaOH溶液,再将剩余的两种溶液分别滴加至红褐色沉淀中,能使沉淀消失的是H2SO4,无明显变化的是NaNO3溶液,故不加其它试剂可以鉴别;
D、Na2CO3均能与HCl、H2SO4反应生成二氧化碳气体,无法鉴别HCl、H2SO4,故不加其它试剂无法鉴别。
故选:C。

 名校课堂系列答案
名校课堂系列答案【题目】小明设计实验探究“锌与硫酸反应快慢的影响因素”实验数据如表
实验编号 | 硫酸的质量分数 | 硫酸的体积/mL | 锌 | 锌的质量/g | 3分钟收集的氢气体积/mL |
① | 20% | 20 | 锌块 | 1 | 31.7 |
② | 20% | 20 | 锌箔 | 1 | 50.9 |
③ | 30% | 20 | 锌块 | 1 | 61.7 |
④ | 30% | 20 | 锌箔 | 1 | 79.9 |
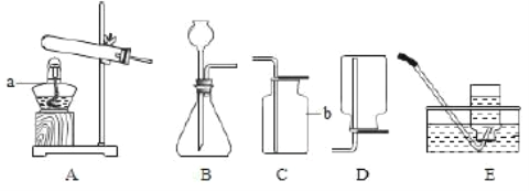
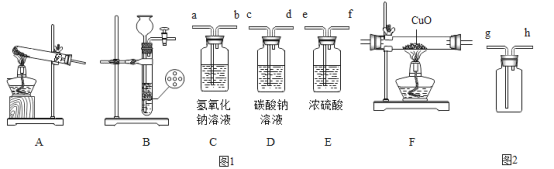
(1)小明做此实验想要验证的假设是______;
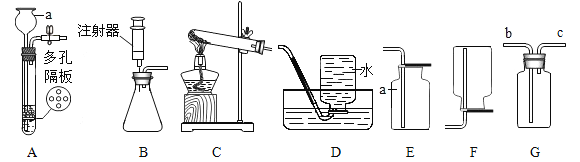
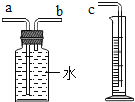
(2)小明用如图装置收集并测量氢气的体积,导管c应与______相连(填“a”或“b”)
(3)如表是小明第①组实验的详细数据:
记录数据时间 | 第1分钟末 | 第2分钟末 | 第3分钟末 | 第4分钟末 | 第5分钟末 | 第6分钟末 |
量筒中水的体积/mL | 3.1 | 19.8 | 31.7 | 41.3 | 48.9 | 54.9 |
已知锌和硫酸反应是放热反应,请据如表数据描述锌与硫酸反应的速率变化情况,并作出合理解释______.
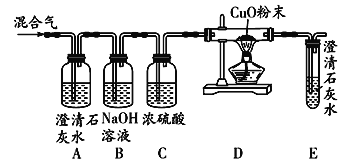
【题目】工业上用废铜料溶于加入氧化剂![]() 如
如![]() 的过氧化氢溶液
的过氧化氢溶液![]() 的稀硫酸得到大量高纯度的硫酸铜。反应过程中产生大量无色无味的气体,某兴趣小组对于该气体的成分进行了如下探究。
的稀硫酸得到大量高纯度的硫酸铜。反应过程中产生大量无色无味的气体,某兴趣小组对于该气体的成分进行了如下探究。
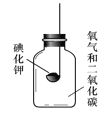
![]() 探究该气体的成分是什么?
探究该气体的成分是什么?
(假设与猜想)
小明认为不可能是二氧化硫,理由是:______;
![]() 小亮认为不可能是氢气,理由是:______;小红认为是氧气。
小亮认为不可能是氢气,理由是:______;小红认为是氧气。
![]() (实验探究)
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
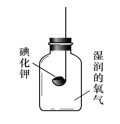
取少量铜屑于试管中,滴加 | 溶液由无色变为 ______ 色,带火星的木 ______ 。 | 该气体是 ______ 。 |
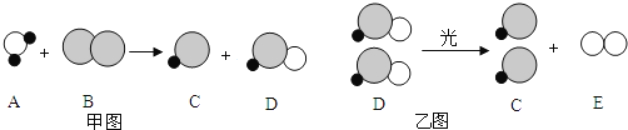
![]() 写出放出气体的反应的化学方程式:______。
写出放出气体的反应的化学方程式:______。
常温下过氧化氢分解缓慢,产生的氧气量很少,不足以使带火星的木条复燃。试通过实验验证是硫酸铜加快了过氧化氢的分解速率,请写出实验设计方案。
实验步骤 | 实验现象 | 实验结论 |
______ | ______ | ______ |