题目内容
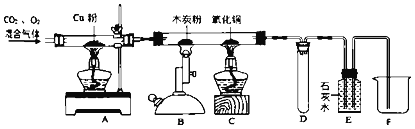
【题目】为了除去二氧化碳中的少量氧气,并探究二氧化碳的性质,某同学设计了如图所示这套装置。
实验步骤 | 实验现象 | 现象分析 |
①点燃A处酒精灯,缓缓通入混合气体 | A中硬质玻璃管内固体 ___,B、C、D无明显现象,E中石灰水变浑浊。 | A硬质玻璃管中铜粉的作用是_____。E中发生反应的化学方程式是___。 |
②点燃B中酒精喷灯 | B中木炭粉减少,E中石灰水浑浊,液面下降。 | B硬质玻璃管中发生反应的化学方程式是_____。 |
③点燃C中酒精灯 | C中现象___,E中石灰水变澄清,液面下降 | C硬质玻璃管中发生反应的化 学方程式是__ |
④停止通入混合气体,并用止水夹夹紧进气口,熄灭A,B,C处的酒精灯和酒精喷灯 | ___ 处有液体导入(填A﹣F) | D装置的作用是__ |
【拓展与思考】
(1)从步骤②开始E中液面开始下降的原因:_____
(2)有同学认为该装置需要添加尾气处理理装置,你认为是否需要并说明理由:_____。
【答案】 逐渐变成黑色 除去混合气中的氧气 CO2+Ca(OH)2=CaCO3↓+H2O CO2+C![]() 2CO 黑色固体逐渐变成红色 CuO+CO
2CO 黑色固体逐渐变成红色 CuO+CO![]() Cu+CO2 D 防止倒吸 E装置收集一氧化碳,防止污染空气 不需要,因为过量一氧化碳已收集在D中,并没有排放到空气中,不会造成污染。
Cu+CO2 D 防止倒吸 E装置收集一氧化碳,防止污染空气 不需要,因为过量一氧化碳已收集在D中,并没有排放到空气中,不会造成污染。
【解析】本题考查了二氧化碳、一氧化碳的化学性质,化学实验方案设计与评价和化学方程式的书写。
①在加热的条件下氧气和铜反应生成氧化铜,所以现象是逐渐变成黑色;A硬质玻璃管中铜粉的作用是除去混合气中的氧气;二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水。E中发生反应的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O;
②在B硬质玻璃管中,碳和二氧化碳在高温的条件下生成一氧化碳,化学方程式为:CO2+C![]() 2CO;
2CO;
③一氧化碳和氧化铜在高温的条件下生成铜和二氧化碳,现象是黑色固体逐渐变成红色,反应的化学方程式是CuO+CO![]() Cu+CO2;
Cu+CO2;
④停止通入混合气体,并用止水夹夹紧进气口,熄灭A,B,C处的酒精灯和酒精喷灯,玻璃管中气压减小,E中的液体倒吸至D中,所以D装置的作用是防止倒吸;
拓展与思考:(1)二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,一氧化碳不会与氢氧化钙反应,难溶于水,所以步骤②开始E中液面开始下降的原因:E装置收集一氧化碳,防止污染空气;
(2)该装置不需要添加尾气处理装置,因为过量一氧化碳已收集在D中,并没有排放到空气中,不会造成污染。