题目内容
【题目】某实验小组利用粗盐通过初步的处理除去其中的难溶性杂质,再将提纯得到的精盐配制100g溶质质量分数为18%的氯化钠溶液。
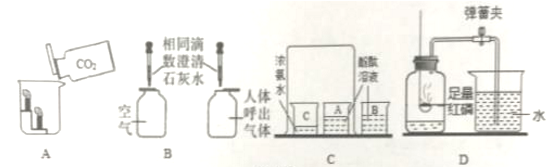
实验I粗盐提纯下图所示为粗盐提纯的主要操作。
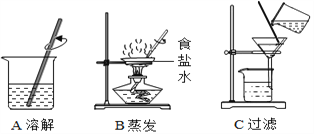
(1)粗盐提纯的主要操作顺序为_________________(填字母序号)。
(2)以上A、B、C实验操作中都用到了玻璃棒。玻璃棒在上述操作中的作用依次是__________、搅拌,使液体受热均匀防止迸溅、_____________。
(3)蒸发时,当出现大量晶体还剩少量水时应停止加热,其目的是_____________。
实验Ⅱ溶液配制
(4)配制上述质量分数的氯化钠溶液用到的主要玻璃仪器__________、烧杯、玻璃棒、胶头滴管。
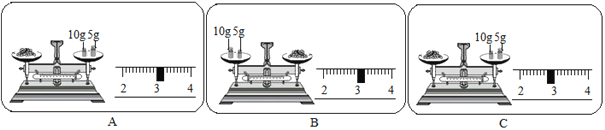
(5)称量氯化钠的质量读数如下图所示,其中正确的是_____________。(填字母序号)
(6)把配好的溶液装入试剂瓶,塞好橡皮塞并_____________,放到指定的地方。
(7)若实验中所配制溶液中的氯化钠溶质质量分数偏低,其原因可能是______(填字母序号)。
A.将称好的固体转移至烧杯时有部分固体洒落桌面; B.溶解时用玻璃棒充分搅拌
C.转移配制好的溶液时溅在试剂瓶外; D.提纯的精盐中仍含有少量可溶性杂质
【答案】 ACB 搅拌,加速溶解 引流 利用余温蒸发水分 量筒 A 贴上标签 AD
【解析】本题考查了氯化钠与粗盐提纯和一定溶质质量分数的溶液的配制。
(1)粗盐提纯的主要操作顺序为溶解、过滤、蒸发,故选ACB;
(2)玻璃棒在上述操作中的作用分别是搅拌,加速溶解,防止液体飞溅、引流;
(3)蒸发时,当出现大量晶体还剩少量水时应停止加热,其目的是利用余温蒸发水分;
(4)配制上述质量分数的氯化钠溶液用到的主要玻璃仪器、量筒、烧杯、玻璃棒、胶头滴管。
(5)需要氯化钠质量为:100g×18%=18g,称量氯化钠时,两盘中应该放等大的纸,并且应该是左物右码,砝码15克,游码放在3克(游码的左端对准刻度“3”),正确的是A。
(6)将配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签,放到指定的地方。
(7) A、将固体转移至烧杯时洒落桌面,会导致溶质质量偏小,从而会导致氯化钠质量分数偏小;B、溶解时用玻璃棒充分搅拌,加速溶解,不影响溶质质量分数;C、转移配制好的溶液时溅在试剂瓶外,不影响溶质质量分数; D、提纯的精盐中仍含有少量可溶性杂质,会导致氯化钠质量偏小,从而导致氯化钠质量分数偏小。故选AD。

 阅读快车系列答案
阅读快车系列答案【题目】(10分)兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验:
(1)氢氧化钠固体要密封保存,原因有:
① ;② 。
【对固体猜想】
猜想一:全部是NaOH;猜想二:全部是Na2CO3;猜想三:是NaOH和Na2CO3混合物
【实验和推断】(2)为进一步确定成分,进行了以下探究:
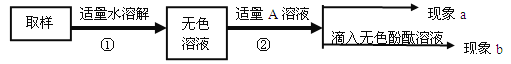
对无色溶液进行以下实验:
实验操作 | 实验现象 | 实验结论 |
第一步: 用试管取约2mL该溶液,滴入适量氢氧化钙溶液,振荡。 | 现象a:白色沉淀 | 化学方程式: ① , 有碳酸钠并全部除尽。 |
第二步: 静置,取上层清液于试管中滴入酚酞溶液,振荡。 | 现象b: ② | 含有NaOH,猜想三成立,是NaOH和Na2CO3混合物 |
③分析:小组中有同学提出质疑,认为以上实验不能证明猜想三成立,理由是:
。
④反思:把第一步中的氢氧化钙溶液换成 溶液,可达到实验目的。
(3)请利用以下提供的试剂,设计实验证明猜想一是正确的,即氢氧化钠没有变质。
提供的试剂有:酚酞溶液、稀盐酸、氢氧化钡溶液、氯化钡溶液
实验操作 | 实验现象 | 实验结论 |
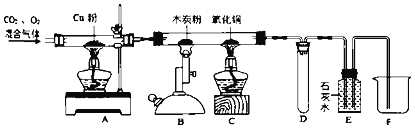
【题目】为了除去二氧化碳中的少量氧气,并探究二氧化碳的性质,某同学设计了如图所示这套装置。
实验步骤 | 实验现象 | 现象分析 |
①点燃A处酒精灯,缓缓通入混合气体 | A中硬质玻璃管内固体 ___,B、C、D无明显现象,E中石灰水变浑浊。 | A硬质玻璃管中铜粉的作用是_____。E中发生反应的化学方程式是___。 |
②点燃B中酒精喷灯 | B中木炭粉减少,E中石灰水浑浊,液面下降。 | B硬质玻璃管中发生反应的化学方程式是_____。 |
③点燃C中酒精灯 | C中现象___,E中石灰水变澄清,液面下降 | C硬质玻璃管中发生反应的化 学方程式是__ |
④停止通入混合气体,并用止水夹夹紧进气口,熄灭A,B,C处的酒精灯和酒精喷灯 | ___ 处有液体导入(填A﹣F) | D装置的作用是__ |
【拓展与思考】
(1)从步骤②开始E中液面开始下降的原因:_____
(2)有同学认为该装置需要添加尾气处理理装置,你认为是否需要并说明理由:_____。
【题目】在中医诊所里,王同学看到老中医用“酒火疗法”为患者治疗,发现白酒竟然能够被点燃。医生告诉她:酒精体积分数较大(即度数较高)的白酒才能被点燃。王同学用体积分数为75%的酒精溶液(指每100L酒精的水溶液中含75mlL酒精)代替白酒进行了系列探究。
【提出问题】能被点燃的酒精溶液的最小体积分数是多少?
【查阅资料】①酒精(C2H5OH)是一种无色液体,易挥,易燃烧,可与水以任意比例互溶。②两种液体混合时,分子间隔不同对混合后的总体积有影响,但对本实验的影响很小,忽略不计。
【实验探究】实验用品:75%酒精溶液、蒸馏水、小烧杯、胶头滴管、量筒(50mL、20mL、10mL)蒸发皿、玻璃棒、火柴。
(1)用75%酒精溶液配制10mL60%的酒精溶液。实验时,最好选用_____mL量筒,使用量筒量取液体读数时应____________。
(2)在室温(20℃)时,王同学按上述方法配制了体积分数为50%、40%、30%、20%的酒精溶液各10mL,分别倒入蒸发皿中,点燃,观察。实验结果如下表
酒精体积分数 | 50% | 40% | 30% | 20% |
观察到的现象 | 可燃 | 可燃 | 不可燃 | 不可燃 |
酒精完全燃烧的化学方程式为____________________。
(3)室温(20℃),张同学在王同学实验探究的基础上,认为35%的酒精溶液不能被点燃,李同学则不同意张同学的观点,你认为李同学的不同意的理由是______________。
(4)拓展应用
①未盖灯帽且久置不用的酒精灯,常常不易被点燃。其原因是________________。
②乙醇汽油就是在汽油中加入适量乙醇混合而成的一种燃料。国家决定推广使用乙醇汽油。下列叙述中,正确的是_______________(选填字母序号)。
A.乙醇汽油是一种新型化合物; B.汽车使用乙醇汽油能减少有害气体的排放;
C.每个乙醇分子中碳、氢、氧三种元素的质量分数之比为C:H:O=12:3:8
【题目】小明同学对家中久置的袋装固体食品防腐剂的成分产生了兴趣(品名和成分如图所示),于是和同学一起,设计实验进行探究:

[提出问题]久置固体食品防腐剂的成分是什么?
[查阅资料]铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
[作出猜想]久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3 。
[实验探究]甲同学的探究方案如下表:
实验操作 | 实验现象 | 实验结论 |
(1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红。 | 固体中一定含有_______和氢氧化钙。此过程的化学方程式_______。 |
(2)另取少量固体放于试管中,滴加足量的稀盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液。 | 固体中一定含有Fe ,一定不含 Fe2O3 |
(3)将步骤(2)中产生的气体通入到澄清的石灰水中 | ________ | 固体中一定含有CaCO3 |
[交流与反思]
(1)“504双吸剂”中的铁粉可以吸收空气中的_______、______。
(2)实验操作(2)的实验现象里“有大量无色气体产生”, 根据甲同学的整体探究方案推测,无色气体的成分是一定含有______,可能含有________。
(3)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是______。
(4)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是_______。