题目内容
根据如图,根据如图装置图,回答有关问题:
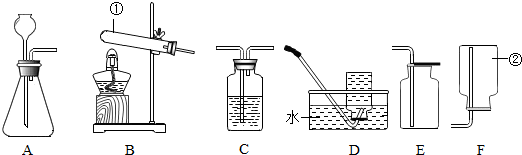
(1)写出装置中标号仪器的名称:① ;② .
(2)写出用实验室用A装置制取氧气的化学方程式: ,并据此选择如图中 (填字母)组装一套制取干燥氧气的装置.
(3)甲烷是密度小于空气、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷.制取甲烷的发生装置应选择 (填装置编号,下同),收集装置应选 ;请写出甲烷完全燃烧的化学方程式 .
(4)向50.0g8%的氢氧化钠溶液中加入一定量的稀硫酸恰好完全反应,此时溶液pH=7.
①求反应前氢氧化钠溶液中溶质的质量;
②求反应后生成硫酸钠的质量.

(1)写出装置中标号仪器的名称:①
(2)写出用实验室用A装置制取氧气的化学方程式:
(3)甲烷是密度小于空气、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷.制取甲烷的发生装置应选择
(4)向50.0g8%的氢氧化钠溶液中加入一定量的稀硫酸恰好完全反应,此时溶液pH=7.
①求反应前氢氧化钠溶液中溶质的质量;
②求反应后生成硫酸钠的质量.
考点:氧气的制取装置,气体的干燥(除水),氧气的收集方法,根据化学反应方程式的计算
专题:有关化学方程式的计算,常见气体的实验室制法、检验、干燥与净化
分析:(1)认识常见仪器的名称;(2)明确实验室中制取氧气装置的选择依据;(3)反应物的状态和反应条件确定了气体的制取装置,甲烷燃烧生成水和二氧化碳;(4)根据“溶液质量×溶质质量分数=溶液中溶质的质量”就可计算出反应前氢氧化钠溶液中溶质的质量;
根据氢氧化钠与硫酸反应的化学方程式和参与反应的NaOH的质量,列出比例式,就可计算出反应后生成硫酸钠的质量.
根据氢氧化钠与硫酸反应的化学方程式和参与反应的NaOH的质量,列出比例式,就可计算出反应后生成硫酸钠的质量.
解答:解:(1)仪器①是试管;②是集气瓶;故填:试管;集气瓶;
(2)A装置适用于固液常温下来制取氧气,则是用二氧化锰作催化剂,分解过氧化氢溶液制取氧气;制取的氧气中混有水蒸气,则再通过盛有浓硫酸的C装置来进行干燥,最后用向上排空气法来进行收集;故填:2H2O2
2H2O+O2↑;ACE;
(3)从题意中知道,该反应的反应物是无水醋酸钠和碱石灰的固体混合物,反应条件是加热,所以发生装置因选用A;生成的甲烷是密度小于空气、难溶于水的气体,所以应选用向下排空气法或排水法,甲烷在氧气中燃烧生成二氧化碳和水,反应的化学方程式为CH4+2O2
CO2+2H2O;
.故填:B;D或F;CH4+2O2
CO2+2H2O;
(4)①反应前氢氧化钠溶液中溶质的质量=50.0g×8.0%=4.0g;
②设反应后生成硫酸钠的质量为x,
2NaOH+H2SO4═Na2SO4+2H2O
80 142
4.0g x
=
x=7.1g
答:(1)反应前氢氧化钠溶液中溶质的质量为4.0g;
(2)反应后生成硫酸钠的质量为7.1g.
(2)A装置适用于固液常温下来制取氧气,则是用二氧化锰作催化剂,分解过氧化氢溶液制取氧气;制取的氧气中混有水蒸气,则再通过盛有浓硫酸的C装置来进行干燥,最后用向上排空气法来进行收集;故填:2H2O2
| ||
(3)从题意中知道,该反应的反应物是无水醋酸钠和碱石灰的固体混合物,反应条件是加热,所以发生装置因选用A;生成的甲烷是密度小于空气、难溶于水的气体,所以应选用向下排空气法或排水法,甲烷在氧气中燃烧生成二氧化碳和水,反应的化学方程式为CH4+2O2
| ||
.故填:B;D或F;CH4+2O2
| ||
(4)①反应前氢氧化钠溶液中溶质的质量=50.0g×8.0%=4.0g;
②设反应后生成硫酸钠的质量为x,
2NaOH+H2SO4═Na2SO4+2H2O
80 142
4.0g x
| 80 |
| 142 |
| 4.0g |
| x |
x=7.1g
答:(1)反应前氢氧化钠溶液中溶质的质量为4.0g;
(2)反应后生成硫酸钠的质量为7.1g.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
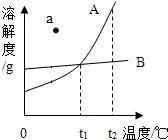 现有A,B两种溶质在水中溶解度曲线如图所示,下列有关描述中不正确的是( )
现有A,B两种溶质在水中溶解度曲线如图所示,下列有关描述中不正确的是( )| A、在温度t2时,A和B配成饱和溶液时溶液的质量分数相同 |
| B、将A的溶液从t2降温到t1时,会析出A溶质晶体 |
| C、当A中混有少量B时,可以配成A较高温下的浓溶液,再进行降温结晶而除去B |
| D、当B中混有少量A时,可以配成B较高温度下的浓溶液再进行蒸发结晶,趁热过滤而除去A |
 如图是市售某牙膏的部分说明.其主要成分是单氟磷酸钠(Na2PO3F),它是牙膏的常用添加剂,实验表明,单氟磷酸钠的质量分数达到0.76%--0.80%时,防龋齿效果较好.(②③小题计算结果精确到0.01%)
如图是市售某牙膏的部分说明.其主要成分是单氟磷酸钠(Na2PO3F),它是牙膏的常用添加剂,实验表明,单氟磷酸钠的质量分数达到0.76%--0.80%时,防龋齿效果较好.(②③小题计算结果精确到0.01%) 2010年上海世博会的场馆建设使用了大量的金属材料.
2010年上海世博会的场馆建设使用了大量的金属材料.