题目内容
为了检验某不纯的碳酸钙样品中碳酸钙的质量分数,取用12.5g样品与足量的稀盐酸反应(杂质不与稀盐酸反应,也不溶于水),充分反应后生成二氧化碳4.4g,求样品中碳酸钙的质量分数.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据二氧化碳的质量可以计算碳酸钙的质量,进一步可以计算碳酸钙的质量分数.
解答:解:设碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 4.4g
=
,
x=10g,
样品中碳酸钙的质量分数为:
×100%=80%,
答:样品中碳酸钙的质量分数为80%.
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 4.4g
| 100 |
| x |
| 44 |
| 4.4g |
x=10g,
样品中碳酸钙的质量分数为:
| 10g |
| 12.5g |
答:样品中碳酸钙的质量分数为80%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
物质的性质决定物质的用途.下列说法中,不合理的是( )
| A、氢气可用于作高能燃料 |
| B、灯泡里充稀有气体可以延长使用寿命 |
| C、氮气用作食品包装袋内的填充气以防腐 |
| D、氧气的化学性质非常活泼,能与所有物质发生化学反应 |
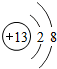 如图为某粒子的结构示意图,下列说法中错误的是
如图为某粒子的结构示意图,下列说法中错误的是