��Ŀ����
 2010���Ϻ�������ij��ݽ���ʹ���˴����Ľ������ϣ�
2010���Ϻ�������ij��ݽ���ʹ���˴����Ľ������ϣ���1����д��һ����ҵ�������Ļ�ѧ����ʽ
��2��������ij��ݽ���ʹ���˴����ĸֲĶ����Ǵ�������Ҫ����Ϊ�ֺʹ���������
��3����ͼ���Ϻ������÷Ͼɽ��������ij��е��ܣ���д�����ַ�ֹ��Щ���ܸ�ʴ�ķ���
��4������ͬѧ�ռ��������������᳡�ݵĽ�����Ƭ���ֱ���ΪX��Y��Z��������X��Y�ֱ����ϡ�����У�Y��Һ����������X����Ӧ����X��Z�ֱ������������Һ�У���һ�������X����������������Zû�б仯����������ʵ����ʵ������ΪX��Y��Z�Ľ������˳��Ϊ
��5���Ϻ���ij�������÷������ᷴӦ������������������1t����м�����ʲ��μӷ�Ӧ����ͬ������9.8t������ǡ�÷�Ӧ�����õ�10.78t����ʣ�����ù������÷��������������Ϊ���٣�
���㣺����ұ��,�й��������������ļ���,�������˳����Ӧ��,������,������ʴ�������������,���ݻ�ѧ��Ӧ����ʽ�ļ���
ר�⣺�������������뻯ѧ����ʽ���ϵļ���,�������������
��������1�����ݹ�ҵ������ԭ������������һ����̼��Ӧ��д����ʽ��
��2�����ݸֵijɷּ��������ʵ��ص�������
��3�����ݸ�ʴ������ԭ���жϷ�ֹ����ʴ�ķ�����
��4�����ݽ������˳�������ã�������֮ǰ�Ľ�������ϡ�����ϡ���ᷴӦ��������������ǰ��Ľ��������ء��ơ����⣩�ɽ����ں���Ľ�����������Һ���û�������
��5�����ݻ�ѧ����ʽ�Ļ�����������Һ���������������ļ��㷽�����㼴�ɣ�
��2�����ݸֵijɷּ��������ʵ��ص�������
��3�����ݸ�ʴ������ԭ���жϷ�ֹ����ʴ�ķ�����
��4�����ݽ������˳�������ã�������֮ǰ�Ľ�������ϡ�����ϡ���ᷴӦ��������������ǰ��Ľ��������ء��ơ����⣩�ɽ����ں���Ľ�����������Һ���û�������
��5�����ݻ�ѧ����ʽ�Ļ�����������Һ���������������ļ��㷽�����㼴�ɣ�
����⣺��1����ҵ������ԭ������������һ����̼��Ӧ�������������̼���䷽��ʽΪ��Fe2O3+3CO
2Fe+3CO2��
��2�����ڸ��к�̼�����ĺϽ����Ըֵ�Ӳ�ȱ���Ҫ��
��3����������ĸ�ʴһ�����������꣬���Կ��Բ��ø�����Ϳ������ڽ�����������һ�������Ӧ�Ľ�������Ĥ�Է�ֹ��������ʴ��
��4�����ݽ������˳�������ã�������֮ǰ�Ľ�������ϡ�����ϡ���ᷴӦ����������X��Y�ֱ����ϡ�����У�Y��Һ����������X����Ӧ�����Խ������y��x������ǰ��Ľ��������ء��ơ����⣩�ɽ����ں���Ľ�����������Һ���û���������X��Z�ֱ������������Һ�У���һ�������X����������������Zû�б仯�����Խ������y��x���ۺϿ�֪���ߵĽ������˳����y��x��z������ͭ�Ļ������������Ա���ǿ������X����������Ӧ�Ļ�ѧ����ʽΪ��Cu+2AgNO3�TCu��NO3��2+2Ag��
��5��������֪ʣ������Dz��������ᷴӦ�����ʣ����Բ��뷴Ӧ������������1t-0.78t=0.22t
����뷴Ӧ�������������x
Fe+H2SO4=FeSO4+H2��
56 98
0.22t x
=
x=0.385t
��ù������÷��������������Ϊ
��100%��3.9%��
�ʴ�Ϊ��
��1��3CO+Fe2O3
2Fe+3CO2��
��2��Ӳ�ȴ�ʴ����ǿ����е�ӹ����ܺõȣ������к�������̼���봿������ɲ�ͬ��
��3�������ᡢͿ�͡����ָ���ȣ�
��4��Y��X��Z��Cu+2AgNO3�TCu��NO3��2+2Ag��
��5���⣺������֪ʣ������Dz��������ᷴӦ�����ʣ����Բ��뷴Ӧ������������1t-0.78t=0.22t
����뷴Ӧ�������������x
Fe+H2SO4=FeSO4+H2��
56 98
0.22t x
=
x=0.385t
��ù������÷��������������Ϊ
��100%��3.9%��
�𣺸ù������÷��������������Ϊ3.9%��
| ||
��2�����ڸ��к�̼�����ĺϽ����Ըֵ�Ӳ�ȱ���Ҫ��
��3����������ĸ�ʴһ�����������꣬���Կ��Բ��ø�����Ϳ������ڽ�����������һ�������Ӧ�Ľ�������Ĥ�Է�ֹ��������ʴ��
��4�����ݽ������˳�������ã�������֮ǰ�Ľ�������ϡ�����ϡ���ᷴӦ����������X��Y�ֱ����ϡ�����У�Y��Һ����������X����Ӧ�����Խ������y��x������ǰ��Ľ��������ء��ơ����⣩�ɽ����ں���Ľ�����������Һ���û���������X��Z�ֱ������������Һ�У���һ�������X����������������Zû�б仯�����Խ������y��x���ۺϿ�֪���ߵĽ������˳����y��x��z������ͭ�Ļ������������Ա���ǿ������X����������Ӧ�Ļ�ѧ����ʽΪ��Cu+2AgNO3�TCu��NO3��2+2Ag��
��5��������֪ʣ������Dz��������ᷴӦ�����ʣ����Բ��뷴Ӧ������������1t-0.78t=0.22t
����뷴Ӧ�������������x
Fe+H2SO4=FeSO4+H2��
56 98
0.22t x
| 56 |
| 98 |
| 0.22t |
| x |
x=0.385t
��ù������÷��������������Ϊ
| 0.385t |
| 9.8t |
�ʴ�Ϊ��
��1��3CO+Fe2O3
| ||
��2��Ӳ�ȴ�ʴ����ǿ����е�ӹ����ܺõȣ������к�������̼���봿������ɲ�ͬ��
��3�������ᡢͿ�͡����ָ���ȣ�
��4��Y��X��Z��Cu+2AgNO3�TCu��NO3��2+2Ag��
��5���⣺������֪ʣ������Dz��������ᷴӦ�����ʣ����Բ��뷴Ӧ������������1t-0.78t=0.22t
����뷴Ӧ�������������x
Fe+H2SO4=FeSO4+H2��
56 98
0.22t x
| 56 |
| 98 |
| 0.22t |
| x |
x=0.385t
��ù������÷��������������Ϊ
| 0.385t |
| 9.8t |
�𣺸ù������÷��������������Ϊ3.9%��
�����������Ƕ��������ص�֪ʶ�Ŀ����⣬����Ĺؼ��Ƕ���ػ���֪ʶ�����������գ������˻���֪ʶ����Ҫ�ԣ�

��ϰ��ϵ�д�
 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д� ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
�����Ŀ

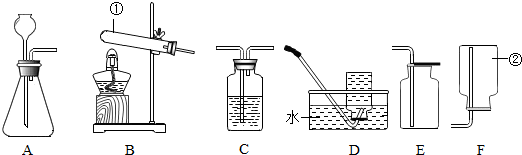
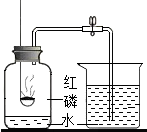
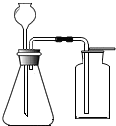 д����ͼװ����ȡ�����һ����ѧ����ʽ
д����ͼװ����ȡ�����һ����ѧ����ʽ