题目内容
 (2009?宣武区二模)A~E是初中化学常见的五种物质,有如下图的转化关系.A是生命之源.“-”表示两端的物质能反应,“→”表示物质间存在转化关系.(部分生成物和反应条件已略去)
(2009?宣武区二模)A~E是初中化学常见的五种物质,有如下图的转化关系.A是生命之源.“-”表示两端的物质能反应,“→”表示物质间存在转化关系.(部分生成物和反应条件已略去)(1)写出下列物质的化学式
B,D.
(2)A生成B反应的基本类型是.
(3)写出下列反应的化学方程式:
B→C.
C→D.
D+E.
【答案】分析:本题从物质没有过多的描述与说明,使得推断变化多端,因此,对“常见的五种物质”的理解则成为本题的一个“着力点”;
常见的酸盐酸和硫酸,常见的碱氢氧化钙和氢氧化钠,常见的盐纯碱碳酸钠、碳酸钙、小苏打碳酸氢钠和氯化钠等,常见的金属氧化物氧化钙、氧化铁和氧化铜,常见的非金属氧化物二氧化碳、一氧化碳、水等;
然后结合“生命之源”的A物质水进行合理地推断.
解答:解:(1)由A是生命之源可确定A为水;水能与可溶性碱对应的金属氧化物反应生成碱,能与非金属氧化物生成对应的酸,结合常见的物质的描述,可推测物质B为常见的金属氧化物氧化钙与水反应生成的常见的碱氢氧化钙;
氢氧化钙可与酸性氧化物、酸生成盐和水,而生成的盐都不是常见的盐;与某些盐反应,生成盐和碱,这类反应中可生成常见的碱氢氧化钠;因此,可推测C为氢氧化钠;
同样地,根据氢氧化钠的性质与所发生的反应进行推断,氢氧化钠可与二氧化碳反应生成常见的盐碳酸钠和水;可推测D物质为碳酸钠;
故答案为:Ca(OH)2;Na2CO3;
(2)A生成B反应即氧化钙和水生成氢氧化钙,由两种物质反应生成一种物质,属于化合反应;
故答案为:化合反应;
(3)B→C,纯碱制烧碱,即氢氧化钙与碳酸钠反应生成氢氧化钠和碳酸钙;
故答案为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
C→D,即由氢氧化钠到碳酸钠,最常见的反应为氢氧化钠与二氧化碳反应生成碳酸钠和水;
故答案为:2NaOH+CO2=Na2CO3+H2O;
D+E,物质E既能与碱物质C氢氧化钠、物质B氢氧化钙,又能与碳酸盐D碳酸钠发生反应,根据常见物质的性质,可推断E为酸,即盐酸或硫酸;所以,D和E的反应即碳酸钠与盐酸或硫酸发生反应生成氯化钠或硫酸钠、水和二氧化碳;
故答案为:Na2CO3+2HCl=2NaCl+CO2↑+H2O(或Na2CO3+H2SO4=Na2SO4+CO2↑+H2O).
点评:对物质的描述或说明越少的推断题,其推断的难度会越大,物质的可能性也越多,在推断时对其可能性不必追求面面俱到穷尽所有结果.
常见的酸盐酸和硫酸,常见的碱氢氧化钙和氢氧化钠,常见的盐纯碱碳酸钠、碳酸钙、小苏打碳酸氢钠和氯化钠等,常见的金属氧化物氧化钙、氧化铁和氧化铜,常见的非金属氧化物二氧化碳、一氧化碳、水等;
然后结合“生命之源”的A物质水进行合理地推断.
解答:解:(1)由A是生命之源可确定A为水;水能与可溶性碱对应的金属氧化物反应生成碱,能与非金属氧化物生成对应的酸,结合常见的物质的描述,可推测物质B为常见的金属氧化物氧化钙与水反应生成的常见的碱氢氧化钙;
氢氧化钙可与酸性氧化物、酸生成盐和水,而生成的盐都不是常见的盐;与某些盐反应,生成盐和碱,这类反应中可生成常见的碱氢氧化钠;因此,可推测C为氢氧化钠;
同样地,根据氢氧化钠的性质与所发生的反应进行推断,氢氧化钠可与二氧化碳反应生成常见的盐碳酸钠和水;可推测D物质为碳酸钠;
故答案为:Ca(OH)2;Na2CO3;
(2)A生成B反应即氧化钙和水生成氢氧化钙,由两种物质反应生成一种物质,属于化合反应;
故答案为:化合反应;
(3)B→C,纯碱制烧碱,即氢氧化钙与碳酸钠反应生成氢氧化钠和碳酸钙;
故答案为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
C→D,即由氢氧化钠到碳酸钠,最常见的反应为氢氧化钠与二氧化碳反应生成碳酸钠和水;
故答案为:2NaOH+CO2=Na2CO3+H2O;
D+E,物质E既能与碱物质C氢氧化钠、物质B氢氧化钙,又能与碳酸盐D碳酸钠发生反应,根据常见物质的性质,可推断E为酸,即盐酸或硫酸;所以,D和E的反应即碳酸钠与盐酸或硫酸发生反应生成氯化钠或硫酸钠、水和二氧化碳;
故答案为:Na2CO3+2HCl=2NaCl+CO2↑+H2O(或Na2CO3+H2SO4=Na2SO4+CO2↑+H2O).
点评:对物质的描述或说明越少的推断题,其推断的难度会越大,物质的可能性也越多,在推断时对其可能性不必追求面面俱到穷尽所有结果.

练习册系列答案
相关题目
(2009?宣武区二模)某固体混合物的主要成分有碳酸钙和氯化钙(氯化钙不与盐酸反应).为探究混合物中碳酸钙的质量分数,甲、乙两个小组同学分别进行了实验:
(1)甲组同学按以下流程进行实验:

①操作A的名称______.
②混合物中碳酸钙的质量分数可能______80% 或______80%(填“>”、“<”或“=”).
(2)乙组的5名同学分别在一个质量为40.00的空烧杯中加入各自称好的固体混合物,然后将质量分数不同的36.50g稀盐酸加入烧杯中,实验数据如表:(假设反应过程中各物质均没有损失)
表中a=______g.
(1)甲组同学按以下流程进行实验:

①操作A的名称______.
②混合物中碳酸钙的质量分数可能______80% 或______80%(填“>”、“<”或“=”).
(2)乙组的5名同学分别在一个质量为40.00的空烧杯中加入各自称好的固体混合物,然后将质量分数不同的36.50g稀盐酸加入烧杯中,实验数据如表:(假设反应过程中各物质均没有损失)
| 组号 | 烧杯及物质的总质量(g) | 稀盐酸溶质质量分数(%) | 产生气体的质量(g) |
| 1 | 42.00 | 2.00 | 0.44 |
| 2 | 45.00 | 5.00 | 1.10 |
| 3 | 44.00 | 9.50 | 1.32 |
| 4 | 46.00 | 9.50 | 1.98 |
| 5 | 44.00 | 6.00 | a |
(2009?宣武区二模)酸、碱、盐是三类重要物质.
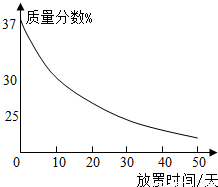
(1)实验室中有一瓶敞口放置的浓盐酸.它的质量分数和放置天数的关系如图.假设水不蒸发,分析浓盐酸的溶质质量分数变化的原因.
(2)观察图片,向小试管内滴加水后,除看到氧化钙固体溶解外,还可观察到的现象是.解释产生此现象的原因;.

(3)如图分别是溴化氢(HBr)和乙醇(C2H5OH)在水中的微观示意图.请你结合已有的酸、碱知识,判断溴化氢的水溶液显,乙醇的水溶液显(填“酸性”、“中性”或“碱性”).

(4)向盛有10mL稀盐酸(其中滴有少量指示剂)的烧杯中加入氢氧化钠溶液,用pH计测定溶液的pH,所得数据如下.请分析并回答下列问题:
①若滴加的指示剂是紫色石蕊溶液,当加入氢氧化钠溶液的体积为13mL时,溶液显色.
②若滴加指示剂是无色酚酞溶液,入氢氧化钠溶液充分振荡后,溶液颜色无变化.此时溶液中的溶质一定有(填化学式);可能有.
(1)实验室中有一瓶敞口放置的浓盐酸.它的质量分数和放置天数的关系如图.假设水不蒸发,分析浓盐酸的溶质质量分数变化的原因.

(2)观察图片,向小试管内滴加水后,除看到氧化钙固体溶解外,还可观察到的现象是.解释产生此现象的原因;.

(3)如图分别是溴化氢(HBr)和乙醇(C2H5OH)在水中的微观示意图.请你结合已有的酸、碱知识,判断溴化氢的水溶液显,乙醇的水溶液显(填“酸性”、“中性”或“碱性”).

(4)向盛有10mL稀盐酸(其中滴有少量指示剂)的烧杯中加入氢氧化钠溶液,用pH计测定溶液的pH,所得数据如下.请分析并回答下列问题:
| 加入NaOH溶液的体积/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.5 | 7.0 | 11.0 | 12.0 |
②若滴加指示剂是无色酚酞溶液,入氢氧化钠溶液充分振荡后,溶液颜色无变化.此时溶液中的溶质一定有(填化学式);可能有.
