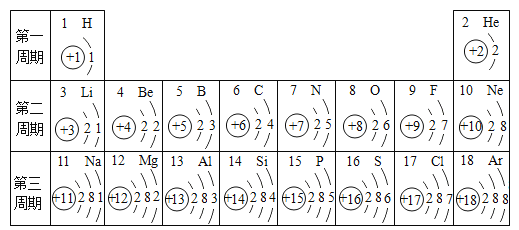
题目内容
【题目】我们用化学学科认识事物的方式全面了解认识“空气”。
(1)从物质分类角度:新鲜的空气属于________(填“混合物”或“纯净物”)
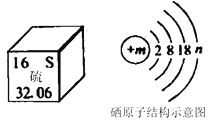
(2)从构成物质的微粒角度用“○”表示氧原子,“●”表示氮原子
①用“![]() ”可表示的微粒是________
”可表示的微粒是________
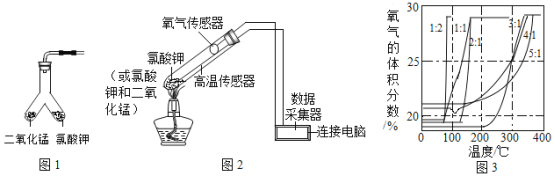
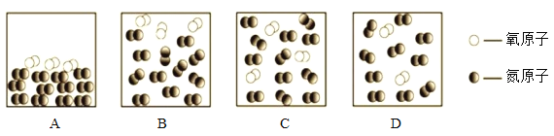
②同温度下,气体的体积比等于分子数目比。若空气中其他成分忽略不计,下列可表示空气微观模型的是__________(填序号)
(3)从环保角度:下列做法有利于净化空气的是_________(填序号)
①使用清洁能源代替煤和石油 ②多使用“共享单车”
③实施绿化工程,减少扬尘污染 ④分类回收垃圾,并露天焚烧
(4)如图为一款新型环保车,可通过 360°旋转的“大炮筒”向四周喷水,从而缓解极端恶劣天气给人带来的不适。分析这款环保车喷水的作用是________

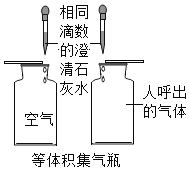
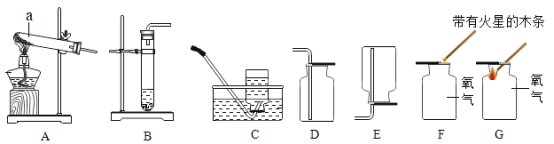
(5)实验探究角度:如图所示的实验进行空气成分的测定。
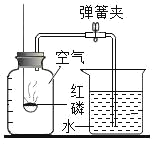
①实验前,应首先检查__________确保实验成功。
②写出红磷燃烧的化学方程式________该实验中红磷应取过量的原因________
③实验中,待集气瓶冷却至室温时,打开弹簧夹,观察到的现象是________
④该实验中能不能用木炭代替红磷,并说明理由________
【答案】混合物 O2或氧分子 C ①②③ 降低空气中的粉尘(答案合理即可) 装置的气密性 4P+5O2![]() 2P2O5 装置内空气中的氧气反应完全 烧杯中的水进入集气瓶中,且占集气瓶容积的五分之一 不能,木条燃烧生成二氧化碳气体,瓶内压强变化不明显。
2P2O5 装置内空气中的氧气反应完全 烧杯中的水进入集气瓶中,且占集气瓶容积的五分之一 不能,木条燃烧生成二氧化碳气体,瓶内压强变化不明显。
【解析】
(1)空气中含有氮气、氧气等多种物质属于混合物;
(2)图A错误,空气中氮气和氧气应该均匀混合;图B错误,空气中氮气和氧气应该均匀混合;图C正确,空气中的氮气和氧气均匀混合,且氧气与氮气的分子个数比为1:4;图D错误,氧气与氮气的分子个数比为1:5;
(3)从环保角度:下列做法有利于净化空气的是①使用清洁能源代替煤和石油,减少二氧化碳的排放②多使用“共享单车”出行,减少汽车尾气的排放③实施绿化工程,减少扬尘污染 ④露天焚烧垃圾会产生有毒有害气体,不利于净化空气。
(4)降低空气中的粉尘,增加空气湿度。(答案合理即可)
(5)做测定空气中氧气含量的实验前,一定要检查装置的气密性;红磷在氧气点燃反应原理是:4P+5O2![]() 2P2O5;红磷应取过量是为了保证集气瓶内的氧气全部反应完全,使实验结果测量更准确;烧杯中的水进入集气瓶中,且占集气瓶容积的五分之一;实验中不能吧红磷换成木炭,木炭燃烧生成二氧化碳气体,瓶内压强变化不明显。
2P2O5;红磷应取过量是为了保证集气瓶内的氧气全部反应完全,使实验结果测量更准确;烧杯中的水进入集气瓶中,且占集气瓶容积的五分之一;实验中不能吧红磷换成木炭,木炭燃烧生成二氧化碳气体,瓶内压强变化不明显。

【题目】课本“分解过氧化氢制氧气的反应中二氧化锰的催化作用”以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
(提出问题)氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
(实验探究)
实验步骤 | 实验现象 |
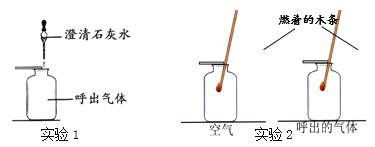
Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag。 | |
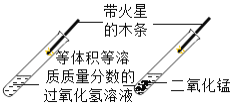
Ⅳ.分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 |
(实验结论)
(1)A中产生的气体是_____________。
(2)实验Ⅱ、Ⅲ证明:氧化铁的___________和____________在反应前后均没有发生变化,可以作过氧化氢溶液分解的催化剂。
(3)写出氧化铁催化过氧化氢溶液分解的符号表达式__________________________。
(实验评价)
(1)实验设计Ⅳ的目的是__________________________________________。
(2)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是_______。
(实验拓展)
(1)查阅资料得知:CuO、CuSO4、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是______________(填序号)。
A.MnO2只能作过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其他反应的反应物或生成物
(2)实验创新是中学生最为重要的科学素养。下图是某学校的师生对“MnO2催化H2O2溶液分解实验装置的创新设计”,实验过程如下:
①将一支球形干燥管水平放置,用滴管吸取3ml(密度为1g/ml)质量分数为5%的H2O2加入干燥管的球泡内,再用药匙取0.2gMnO2粉末,加在干燥管的进气管的管壁上。
②点燃橡胶塞上棒香后,塞紧干燥管并将其竖立,观察到带火星的棒香立即复燃。
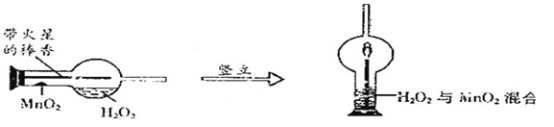
对该创新实验的评价,你认为不合理的是_________(填序号)。
A.实验中所用的仪器、材料及药品均易得到
B.实验使用的药品用量太大
C.反应速度太慢,耽误时间
D.实验现象明显,整个装置好似点燃的灯塔,趣味性强