题目内容
【题目】对化学方程式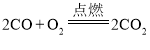 ,所能表达的意义,下列说法错误的是
,所能表达的意义,下列说法错误的是
A. CO和![]() 在点燃的条件下生成二氧化碳
在点燃的条件下生成二氧化碳
B. 参加反应的CO、![]() 与生成的
与生成的![]() 的分子个数比是2:1:2
的分子个数比是2:1:2
C. 此方程式还能表示参加反应的碳、氧原子内部的变化过程
D. 每56份质量的CO和32份质量的![]() 在点燃的条件下生成88份质量的
在点燃的条件下生成88份质量的![]()
【答案】C
【解析】
A、根据化学方程式可知,CO和![]() 在点燃的条件下生成二氧化碳,故A正确,不符合题意;
在点燃的条件下生成二氧化碳,故A正确,不符合题意;
B、根据化学方程式可知,参加反应的CO、![]() 与生成的
与生成的![]() 的分子个数比是2:1:2,故B正确,不符合题意;
的分子个数比是2:1:2,故B正确,不符合题意;
C、化学方程式可表示:反应物和生成物的种类;反应的条件;反应物和生成物的微观粒子个数比;反应物和生成物的质量比。此方程式不能表示参加反应的碳、氧原子内部的变化过程,故C错误,符合题意;
D、根据化学方程式可知, 每56份质量的CO和32份质量的![]() 在点燃的条件下生成88份质量的
在点燃的条件下生成88份质量的![]() ,故D正确,不符合题意。故选C。
,故D正确,不符合题意。故选C。

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
【题目】化学兴趣小组的同学欲测定实验室中某合金黄铜样品中铜的质量分数(不考虑黄铜中的其他杂质),请你参与他们的探究过程。
查阅资料:(1)合金是由一种金属元素跟其他金属或非金属元素熔合而成的、具有金属特性的物质。合金的种类很多,用途非常广泛,黄铜是铜(Cu)和锌(Zn)的合金,它可以用来制造机器和电器的零件等。
(2)铜与稀盐酸不反应,锌与稀盐酸发生的化学反应为:![]() 。
。
实验探究:称量10g粉末状黄铜样品放入烧杯中,量取45mL稀盐酸分三次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
第一次 | 第二次 | 第三次 | |
加入稀盐酸的体积(ml) | 15 | 15 | 15 |
生成氢气的质量(g) | 0.04 | 0.04 | 0.02 |
试求;此黄铜样品中铜的质量分数是多少?____(写出计算过程,质量分数用百分数表示。)