题目内容
【题目】实验室中有一瓶标签受损的无色液体,如图所示。这瓶无色液体是什么呢?实验员老师告诉大家,该液体可能是过氧化氢溶液、稀盐酸、稀硫酸和蒸馏水中的一种。
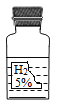
(1)大家讨论后一致认为不可能是蒸馏水,理由是_____;同时也不可能是稀盐酸,理由是_____。
(2)为确定该液体成分,同学们继续进行了如下实验探究:
实验操作 | 实验现象 | 实验结论 |
步骤一:取该液体适量于试管中,向其中加入_____ | _____ | 该液体不是过氧化氢溶液。 |
步骤二:_____ | _____ | 该液体是稀硫酸 |
(反思交流)
①大家认为标签受损的原因可能是_____;
②如果该液体是过氧化氢溶液,则步骤一中产生的变化用化学方程式表示为_____。
【答案】由标签知该液体是混合物,而蒸馏水为纯净物 盐酸中氯化氢的化学式的氢元素的右下角不会有2 二氧化锰 没有气泡产生 取该液体适量于试管中,向其中滴加紫色石蕊试液。 石蕊试液变红色 倾倒液体时标签未朝向手心 
【解析】
(1)由标签可知该液体是混合物,而蒸馏水为纯净物,所以不可能是蒸馏水;盐酸中的溶质是氯化氢,它的化学式是HCl,氢元素的右下角没有2;故填:由标签知该液体是混合物,而蒸馏水为纯净物;盐酸中氯化氢的化学式的氢元素的右下角不会有2。
(2)步骤一:根据该液体不是过氧化氢溶液的结论,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,若不产生气体,则该液体不是过氧化氢溶液,所以是向液体中加入二氧化锰,现象是没有气泡产生;故填:二氧化锰;没有气泡产生。
步骤二:根据结论该液体是稀硫酸,可知溶液显酸性,能使紫色的石蕊试液变成红色;因此可取该液体适量于试管中,向其中滴加紫色石蕊试液,石蕊试液变红色即可证明。故填:取该液体适量于试管中,向其中滴加紫色石蕊试液;石蕊试液变红色。
(3)倾倒液体药品时,标签要向着手心,防止残留的液体腐蚀标签,故填:倾倒液体时标签未朝向手心。
(4)过氧化氢能在二氧化锰的催化作用下快速的生成氧气和水,故反应的方程式为: ,故填:
,故填: 。
。

【题目】镓元素的单质是半导体材料,其原子结构示意图及在元素周期表中的信息如图,从图中获得的信息错误的是
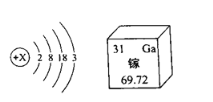
A. X=31
B. 镓属于非金属元素
C. 镓的相对原子质量是69.72
D. 镓原子核外有4个电子层
【题目】黄铜是铜和锌的合金。某化学兴趣小组的同学欲测定实验室中某黄铜样品中铜的质量分数(不考虑黄铜中的其他杂质),请你参与他们的探究过程。称量10g粉末状黄铜样品放入烧杯中,量取45mL稀硫酸分三次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
第一次 | 第二次 | 第三次 | |
加入稀硫酸的体积(mL) | 15 | 15 | 15 |
生成氢气的质量(g) | m | 0.04 | 0.02 |
试求:
(1)m的数值_____。
(2)此黄铜样品中铜的质量分数是少?_____(写出计算过程)