题目内容
【题目】溶液与人类生产、生活密切相关,请根据要求回答相关问题。
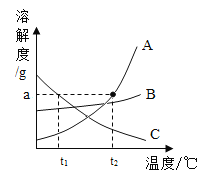
(1)A、B、C三种固体物质的溶解度曲线如图所示。
①![]() 时,A、B、C三种物质的溶解度由小到大的顺序是_____。
时,A、B、C三种物质的溶解度由小到大的顺序是_____。
②A、B、C三种物质中,溶解度随受温度影响较小的是_____。
③![]() 时,完全溶解agA物质最少需要水的质量是_____g。
时,完全溶解agA物质最少需要水的质量是_____g。
④![]() 时,A饱和溶液的溶质质量分数_____B饱和溶液溶质质量分数(填“大于”、“等于”或“小于”)
时,A饱和溶液的溶质质量分数_____B饱和溶液溶质质量分数(填“大于”、“等于”或“小于”)
(2)实验室欲除去粗盐样品中含有的不溶性泥沙,在过滤操作中需要用到的实验仪器和用品有:烧杯、铁架台(带铁圈)、漏斗、_____和滤纸。
(3)在实验室中,配制溶质质量分数为9%的氯化钠溶液100g,需要氯化钠固体的质量是_____g。将100g9%的氯化钠溶液配成含氯化钠为0.9%的溶液,需加入蒸馏水的质量至少是_____g。
【答案】C>B>A B 100 大于 玻璃棒 9 900
【解析】
(1)①![]() 时,A、B、C三种物质的溶解度由小到大的顺序是C>B>A;
时,A、B、C三种物质的溶解度由小到大的顺序是C>B>A;
②溶解度曲线越平缓,该物质溶解度受温度影响越小,故A、B、C三种物质中,溶解度受温度影响较小的是B;
③![]() 时,A物质溶解度为ag,即100g水中最多能溶解ag A物质,故完全溶解ag A物质最少需要100g水;
时,A物质溶解度为ag,即100g水中最多能溶解ag A物质,故完全溶解ag A物质最少需要100g水;
④![]() 时,A物质的溶解度大于B物质的溶解度,一定温度下饱和溶液的溶质质量分数=
时,A物质的溶解度大于B物质的溶解度,一定温度下饱和溶液的溶质质量分数=![]() ,故配成饱和溶液时,A物质饱和溶液的溶质质量分数大于B物质的;
,故配成饱和溶液时,A物质饱和溶液的溶质质量分数大于B物质的;
(2)过滤操作中需要用到的实验仪器和用品有:烧杯、铁架台(带铁圈)、漏斗、玻璃棒和滤纸;
(3)在实验室中,配制溶质质量分数为9%的氯化钠溶液100g,需要氯化钠固体的质量是![]() ;100g9%的氯化钠溶液中,含溶质
;100g9%的氯化钠溶液中,含溶质![]() ,要配成含氯化钠为0.9%的溶液,则稀释后溶液总质量为
,要配成含氯化钠为0.9%的溶液,则稀释后溶液总质量为![]() ,需要加水的质量为
,需要加水的质量为![]() 。
。

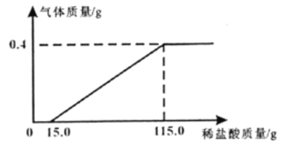
【题目】某研究小组为探究“铁丝和盐酸反应的快慢与什么因素有关”,取相同质量的铁丝和足量的盐酸反应得到下表中的三组实验数据,请回答下列问题:
实验编号 | 盐酸的质量分数/% | 反应温度/°C | 铁丝消失的时间/s |
① | 3 | 20 | 300 |
② | 6 | 20 | 200 |
③ | 6 | 40 | 40 |
(1)写出铁丝和盐酸反应的化学方程式:________________。
(2)实验②和③可探究________对铁丝和盐酸反应快慢的影响。若欲探究浓度对铁丝和盐酸反应快慢的影响,应选择的实验编号是____________。
(3)根据上表中的实验数据,可得出的结论是_______(写出一点即可)。
(4)如果把上表中实验②的反应温度改为25°C,请推测铁丝消失的时间t的取值范围:__________。
(5)实验除了用铁丝消失的时间来衡量反应的快慢外,你还能提出新的方法来衡量该反应的快慢吗?你的方法有________(写一点即可)。
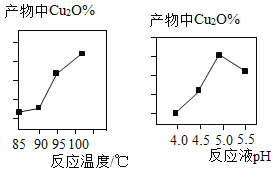
【题目】探究铜生锈的条件
(提出猜想)根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
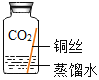
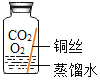
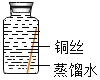
(进行实验)实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
现象 | 无明显现象 | 无明显现象 | 铜丝表面有绿色物质 | 无明显现象 | 无明显现象 |
(解释与结论)
(1)实验中使用“经煮沸迅速冷却的蒸馏水”,其目的是_____。
(2)得出“铜生锈一定与O2有关”的结论,依据的两个实验是_____(填编号)。
(3)对比实验①和③,得出的结论是_____。
(4)为验证猜想,实验⑤广口瓶中除铜丝外,还应有的物质是_____。
(5)由上述实验可推知,铜生锈的条件是_____。
(反思与应用)
(6)结合上述实验,你对保存铜制品的建议是_____。
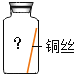
【题目】实验室中有一瓶标签受损的无色液体,如图所示。这瓶无色液体是什么呢?实验员老师告诉大家,该液体可能是过氧化氢溶液、稀盐酸、稀硫酸和蒸馏水中的一种。
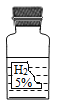
(1)大家讨论后一致认为不可能是蒸馏水,理由是_____;同时也不可能是稀盐酸,理由是_____。
(2)为确定该液体成分,同学们继续进行了如下实验探究:
实验操作 | 实验现象 | 实验结论 |
步骤一:取该液体适量于试管中,向其中加入_____ | _____ | 该液体不是过氧化氢溶液。 |
步骤二:_____ | _____ | 该液体是稀硫酸 |
(反思交流)
①大家认为标签受损的原因可能是_____;
②如果该液体是过氧化氢溶液,则步骤一中产生的变化用化学方程式表示为_____。