题目内容
【题目】现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
次数 | 1 | 2 | 3 | 4 |
加入稀硫酸的质量/g | 35.0 | 35.0 | 35.0 | 35.0 |
剩余固体的质量/g | 6.8 | 5.6 | 4.4 | 4.2 |
求:
(1)该混合物粉末中铜的质量分数 ________ ;
(2)若参加反应的金属为R,请写出R与稀硫酸反应的化学方程式 ________ ;
(3)设金属R的相对原子质量为X,根据已知条件列出求解(X)的比例式 ________ ;
(4)如果将第三次加入硫酸充分反应后的溶液蒸发掉8.3g水,且无晶体析出,则所得溶液中溶质的质量分数为________ .
【答案】52.5%;R+H2SO4═RSO4+H2↑;![]() ;18.0%
;18.0%
【解析】
(1)根据金属活动性顺序表可知,铜不与稀酸反应,再根据表中数据可知,铜的质量为4.2g,则混合物粉末中铜的质量分数=![]() ×100%= 52.5%。
×100%= 52.5%。
(2)铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,故金属R与硫酸反应后均生成+2价的硫酸盐,故反应化学方程式为R+H2SO4═RSO4+H2↑。
(3)设该金属R的相对原子质量为X,通过观察表格可知,第一次反应消耗1.2g的金属R,且稀硫酸被完全消耗,故第一次参加反应的稀硫酸质量是35g,其溶质质量为35g×14%=4.9g。故有:
R+H2SO4═RSO4+H2↑
X98
1.2g4.9g
根据反应物的质量比有比例式:![]() =
=![]() 解得X=24,该金属为金属镁。
解得X=24,该金属为金属镁。
(4)由(3)可知,第三次加入硫酸充分反应后,溶质为MgSO4,参加反应的金属镁的质量为8g-4.4g=3.6g假设溶质质量为x,则有:
Mg+H2SO4═MgSO4+H2↑
24 120 2
3.6g x y
![]() =
=![]() =
=![]() 解得x=18g,y=0.3g,第三次加入硫酸充分反应后,加入稀硫酸质量为35g×3=105g,溶液蒸发掉8.3g水,且无晶体析出,另又生成0.3g氢气,故所得溶液质量为105g+3.6g-8.3g-0.3g=100g。故所得溶液中溶质的质量分数=
解得x=18g,y=0.3g,第三次加入硫酸充分反应后,加入稀硫酸质量为35g×3=105g,溶液蒸发掉8.3g水,且无晶体析出,另又生成0.3g氢气,故所得溶液质量为105g+3.6g-8.3g-0.3g=100g。故所得溶液中溶质的质量分数=![]() ×100%=18%。
×100%=18%。

【题目】超市出现了一种含“污渍爆炸盐”的新产品(如图),能清除衣服上难以清洗的汗 渍、果汁渍。它的特殊的名称让小明对它产生了探究的兴趣。

(1)小明在超市的___区域购买了此产品。
(2)阅读产品标签:“污渍爆炸盐”是一种衣物助洗剂,主要成分是过碳酸钠,能在瞬间去除洗衣液难以除去的多种顽固污 渍……,本产品不伤衣物,无磷是它的一大优点。含磷洗涤剂对环 境的危害是______。
(3)查阅资料:过碳酸钠(Na2CO4)是白色结晶颗粒,溶于水 会产生碳酸盐和其它化合物。
(4)合理猜想其它化合物为:
i. NaOH;ii. H2O2;iii. NaOH 和 H2O2;小明做出以上猜想的理论依据是___。
(5)实验设计:探究“污渍爆炸盐”水溶液的成分,完成下列表格。 已知:Mg(OH)2 是难溶于水的白色固体。
实验步骤 | 实验现象 | 实验结论 |
步骤 1:取少量“污渍爆炸盐”于烧杯中,加入足量蒸馏水,充分搅拌。 | 固体完全溶解,形成无色溶液 | |
步骤 2:取少量步骤 1 形成的溶液于试管中,再加 入___ , 振荡,静置。 | 白色沉淀 | 含有 Na2CO3 |
步骤 3:取少量步骤 2 试管中的上层清液于另一支 试管中,再滴加少量 MgCl2 溶液,振荡。 | 无明显现象 | ___ |
步骤 4:另取一支试管,加入少量步骤 1 形成的溶 液,再加入__ , 将带火星木条伸入试管中。 | ___ | 含有 H2O2 |
(6)实验结论:猜想__ 正确。写出过碳酸钠与水反应的化学方程式:____ 。
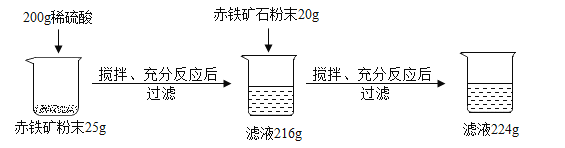
【题目】碲(Te)被誉为“现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁”。实验室模拟提取碲的一个实验是:取某含碲溶液于烧瓶中,加入适量的NaCl,加热到一定温度,持续通入SO2,待反应一段时间,过滤得到粗碲。
(1)反应的总反应方程式为TeOSO4 + 2SO2 + 3__X__ ![]() Te↓+ 3H2SO4,则X为_________(填化学式)
Te↓+ 3H2SO4,则X为_________(填化学式)
(2)为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaCl浓度和SO2流量不变的条件下,进行下述对比试验,数据如下:
实验 | 温度/℃ | 反应时间/h | 粗碲沉淀率/% |
a | 65 | 3.0 | 65.0 |
b | 80 | 3.0 | 98.9 |
c | 80 | 2.0 | 98.9 |
d | 90 | 2.0 | 97.0 |
①该小组研究的反应条件是_________________和_____________。
②实验a和b的目的是______________________________。
③在上述四组实验中,最佳的反应条件是_______℃和_______h。
④为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗碲沉淀率。若再设计对比实验,选择的反应条件还可以是__________(填选项)。
A.80℃,1.5h B.80℃,2.5h C.70℃,2.0h D.95℃,2.0h