题目内容
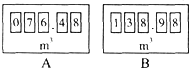
【题目】某同学家的天然气表月头与月末的数字分别如图A、B所示.若天然气的密度是0.76克/升,每立方米的天然气是2元,求:
(1)该同学家这月用去天然气多少立方米?折合人民币多少元?
(2)若天然气中甲烷的质量分数是90%(杂质不燃烧),则该同学家每月在燃烧天然气时消耗氧气的量是多少千克?
【答案】62.5立方米,折合人民币125元,17.1千克.
【解析】
(1)由天然气表月头与月末的数字可知,该同学家这月用去天然气的体积是:138.98m3-76.48m3=62.5m3,折合人民币是62.5m3×2元/m3=125元;
(2)该同学家这月用去天然气的体积是62.5m3=62500L,该同学家每月燃烧天然气中甲烷的质量为:62500L×0.76g/L×90%=4275g=4.275kg,设该同学家每月在燃烧天然气时消耗氧气的质量为x,
CH4 +2O2![]() CO2+2H2O
CO2+2H2O
1664
4.275kgx
![]()
x=17.1kg,
答:(1)该同学家这月用去天然气62.5立方米,折合人民,125元;(2)该同学家每月在燃烧天然气时消耗氧气的量是17.1千克。

【题目】现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
次数 | 1 | 2 | 3 | 4 |
加入稀硫酸的质量/g | 35.0 | 35.0 | 35.0 | 35.0 |
剩余固体的质量/g | 6.8 | 5.6 | 4.4 | 4.2 |
求:
(1)该混合物粉末中铜的质量分数 ________ ;
(2)若参加反应的金属为R,请写出R与稀硫酸反应的化学方程式 ________ ;
(3)设金属R的相对原子质量为X,根据已知条件列出求解(X)的比例式 ________ ;
(4)如果将第三次加入硫酸充分反应后的溶液蒸发掉8.3g水,且无晶体析出,则所得溶液中溶质的质量分数为________ .