题目内容
【题目】元素周期表是学习和研究化学的重要工具,它的内容十分丰富.如图是元素周期表的部分内容,请回答下列问题:
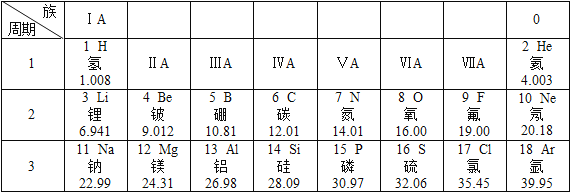
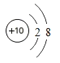
(1)请从如图中查出地壳中含量最多的金属元素的符号___和相对原子质量___.
(2)写出第二周期中的金属元素的名称___、___.
(3)不同元素的本质区别是___.
(4)分析如图,可以看出同一周期的规律是___.
(5)8号元素和13号元素形成化合物的名称为___.
【答案】Al 26.98 锂元素 铍元素 核内质子数不同 原子序数依次递增,最外层电子数由左至右依次递增 氧化铝
【解析】
同一周期,原子序数依次递增,电子层数不变,最外层电子数依次增加,同一族元素,电子层数依次递增,最外层电子数相同。看元素的种类,就看质子数是否相同。
(1)地壳中含量最多的金属元素是铝元素,铝元素的符号是Al,相对原子质量是26.98。
(2)第二周期中的金属元素的名称是锂元素、铍元素。
(3)不同元素的本质区别是核内质子数不同。
(4)分析如图,可以看出同一周期的规律是原子序数依次递增,最外层电子数由左至右依次递增。
(5)8号元素是氧元素、13号元素是铝元素,形成化合物的名称为氧化铝。

 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案【题目】化学科技小组同学将13.9g含杂质的纯碱样品(碳酸钠与氯化钠的混合物)
与90.5g稀盐酸相混合充分反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示:(已知:Na2CO3 +2HCl=2NaCl+CO2↑+H2O)
反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
气体质量m/g | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.4 | 4.4 |
根据题目要求,回答下列问题:
(1)碳酸钠完全反应后,生成CO2的质量为_____g
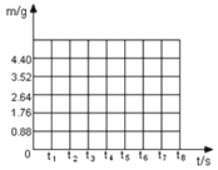
(2)请根据表中数据在下面的坐标图中,画出反应是生成气体的质量(m)随时间(t)变化的曲线。____
(3)求纯碱样品中Na2CO3的质量_____。
(4)反应结束后,溶液中没有剩余固体,则完全反应后溶液中NaCl的质量分数为_____;若要将反应得到的溶液的浓度稀释为10%,则需加入_____g的蒸馏水。
【题目】实验课上,同学们利用澄清石灰水检验空气中的二氧化碳,实验中发现各组石灰水浑浊程度存在较大差异,于是设计实验探究影响石灰水浑浊程度的因素。
(进行实验)装置图如下所示。

实验1:取饱和澄清石灰水进行实验。
实验序号 | 1-1 | 1-2 | 1-3 | 1-4 |
饱和澄清石灰水体积/mL | 2.0 | 1.5 | 1.0 | 0.5 |
缓慢通入2 L空气后的浑浊程度 | 不明显 | 明显 | 非常明显 | 明显 |
实验2:利用向饱和石灰水中添加蒸馏水来调节石灰水浓度进行实验(溶液浓度变化引起的溶液密度变化忽略不计)。
实验序号 | 2-1 | 2-2 | 2-3 | 2-4 |
饱和澄清石灰水体积/mL | 2.0 | 1.5 | 1.0 | 0.5 |
加入蒸馏水体积/mL | 0 | a | b | c |
缓慢通入3 L空气后的浑浊程度 | 非常明显 | 明显 | 不明显 | 无现象 |
(解释与结论)
(1)小试管中发生反应的化学方程式为____________。
(2)实验1的目的为____________。
(3)实验2中a、b、c三处数据,设计合理的是________。
A 0.5 0.5 0.5 B 0.5 1.0 1.5
C 1.0 1.5 2.0 D 1.0 2.0 3.0
(4)实验2的结论是________。
(反思与评价)
(5)通过对比实验1-1和2-1,可得出影响石灰水浑浊程度的另一因素是________,理由是________。