题目内容
【题目】化学科技小组同学将13.9g含杂质的纯碱样品(碳酸钠与氯化钠的混合物)
与90.5g稀盐酸相混合充分反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示:(已知:Na2CO3 +2HCl=2NaCl+CO2↑+H2O)
反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
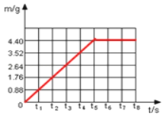
气体质量m/g | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.4 | 4.4 |
根据题目要求,回答下列问题:
(1)碳酸钠完全反应后,生成CO2的质量为_____g
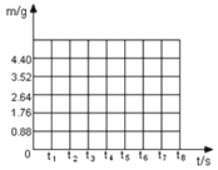
(2)请根据表中数据在下面的坐标图中,画出反应是生成气体的质量(m)随时间(t)变化的曲线。____
(3)求纯碱样品中Na2CO3的质量_____。
(4)反应结束后,溶液中没有剩余固体,则完全反应后溶液中NaCl的质量分数为_____;若要将反应得到的溶液的浓度稀释为10%,则需加入_____g的蒸馏水。
【答案】4.4g 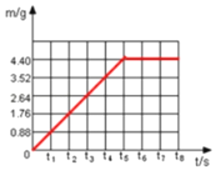 10.6g 15% 50
10.6g 15% 50
【解析】
解:(1)根据图表数据分析可知,生成CO2的质量为4.4g。
(2)根据图表数据,反应生成气体的质量(m)随时间(t)变化的曲线为:
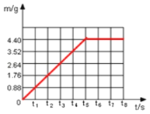
(3)设样品中碳酸钠的质量为x。
![]()
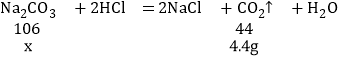
![]()
解得:x=10.6g
答:纯碱样品中Na2CO3的质量为10.6g
(4)设反应生成NaCl的质量为y。
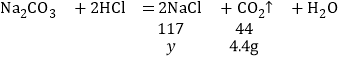
![]() ,解得 y=11.7g
,解得 y=11.7g
样品中氯化钠的质量为13.9g﹣10.6g=3.3g
反应后溶液中溶质的质量=11.7g+3.3g=15g
反应后溶液的质量=13.9g+90.5g﹣4.4g=100g
∴完全反应后所得溶液中溶质的质量分数为![]() ×100%=15%
×100%=15%
稀释前后溶质的质量相等,设若要将反应得到的溶液的浓度稀释为10%,则需加入蒸馏水的质量为z。
(100g+z)×10%=15g
z=50g
答:(1)碳酸钠完全反应后,生成CO2的质量为4.4g;(2)根据图表数据,反应生成气体的质量(m)随时间(t)变化的曲线为:
(3)纯碱样品中Na2CO3的质量为10.6g;(4)反应结束后,溶液中没有剩余固体,则完全反应后溶液中NaCl的质量分数为15%;若要将反应得到的溶液的浓度稀释为10%,则需加入50g的蒸馏水。

 阅读快车系列答案
阅读快车系列答案【题目】某研究性学习小组以“酸与碱能否发生反应”为课题进行了实验探究。
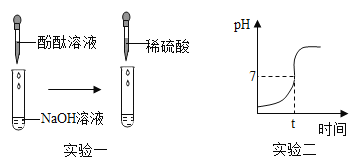
(实验一)
(1)向滴有酚酞试液的NaOH溶液中滴入稀硫酸,观察到溶液颜色由_____,证明硫酸和氢氧化钠发生了反应,该反应的化学方程式为_____。
(2)继续往上述反应后的溶液中逐滴滴入NaOH溶液,不断振荡,如果观察到_____现象,证明了滴加的稀硫酸过量。
(实验二)测量酸和碱反应过程的pH
(1)实验过程中用传感器实时获得溶液的pH,要得到如图所得变化曲线,所进行的操作是_____(填字母)。
A 将稀硫酸溶液逐滴滴加到氢氧化钠溶液中
B 将氢氧化钠溶液逐滴滴加到稀硫酸溶液中
(2)根据如图2溶液pH变化,判断酸和碱发生反应的依据是_____。
(实验三)小组同学经过讨论,一致认为除了上述方法外,还可以按照如表实验方法证明硫酸和氢氧化钠发生了反应。
实验步骤 | 实验现象 | 实验结论 |
取少量氢氧化钠溶液于试管中,加入过量的稀硫酸,再加入少量的氧化铜 | 得到蓝色溶液,无_____ | 氢氧化钠和硫酸发生了化 学反应 |
(拓展延伸)同学们对氢氧化钠溶液和稀硫酸反应后溶液中的溶质成分产生了浓厚的兴趣,于是进行了进一步的探究。
(提出问题)氢氧化钠溶液和稀硫酸反应后溶液中的溶质成分
(提出猜想)猜想一:Na2SO4猜想二:Na2SO4和H2SO4你的合理猜想是:_____。
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
取少量反应后的溶液置于试管中_____ | _____ | 猜想二正确 |
(实验反思)在分析化学反应后所得物质成分时,除考虑生成物外还需要考虑反应物是否有剩余。
【题目】学习了二氧化锰过氧化氢分解有催化作用的知识后,某兴趣小组的同学提出问题:氧化铁能否起到类似于二氧化锰的催化作用呢?于是他们进行了以下探究.
(猜想)
Ⅰ.氧化铁不是反应的催化剂、也不参与反应,质量和化学性质反应前后均不变;
Ⅱ.氧化铁参与反应产生氧气,反应前后质量不变,但化学性质发生了改变;
Ⅲ.氧化铁是反应的催化剂,反应前后_____.
(实验)用天平称0.2g氧化铁,用试管取5mL 5%的过氧化氢溶液,进行如下实验:
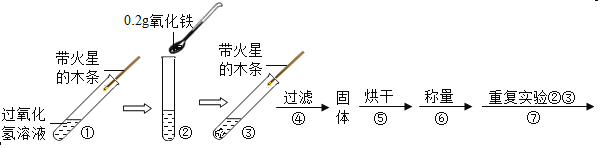
(注:氧化铁不溶于水,过滤可与水分离)
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
带火星的木条复燃. | _____ | 过氧化氢溶液中:_____ | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
(2)步骤①的目的是_____.
(3)写出上述有关过氧化氢分解的文字表达式_____.
(4)步骤⑦重复实验②、③的目的是_____.
(继续探究)从上述实验得出氧化铁是反应的催化剂.对同种催化剂,有哪些因素可能影响催化效果?请提出猜想并设计实验进行探究._____(注意:至少探究两种因素,答对一种因素奖励2分,本題最多奖励4分,化学试卷总分不超过60分)