题目内容
【题目】某班两组同学利用稀硫酸和氢氧化钠溶液进行了如下实验:
(1)第一小组同学测量9.8%的稀硫酸和10%的氢氧化钠溶液中和反应过程中温度的变化。
①第一步:关于溶液的配制和保存
首先,该小组同学将配制好的10%的氢氧化钠溶液,倒入带_____塞的细口瓶中,备用。其次,该组同学用如表标签所示的浓硫酸配制100g溶质质量分数为9.8%的稀硫酸。请列式计算所需水的体积_____。
硫酸
化学式H2SO4
相对分子质量98
质量分数98%
本试剂为无色透明的粘稠液体
有腐蚀性!
②该小组同学量取了8组均为8mL的氢氧化钠溶液,分别向其中加入一定体积的稀硫酸,测得温度变化如表所示:
实验组别 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
加入稀硫酸的体积 (V)/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 |
溶液温度上升 (△t)/℃ | 4.8 | 8.4 | 11.2 | 11.1 | 13.1 | 11.4 | 10.2 | 9.2 |
其中实验组别为_____(填实验组别的序号)的一组数据明显不合理,判断理由是_____。
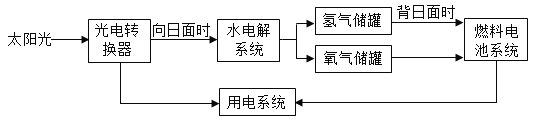
(2)第二小组同学计划探究中和反应过程中的pH变化情况。他们取稀释后的氢氧化钠溶液25g,向其中加入溶质质量分数为9.8%的稀硫酸,加入稀硫酸的质量与溶液pH的变化情况如图所示。计算:

①当两者恰好完全中和时,所得溶液中溶质的质量分数_____。(计算结果精确到0.1%)
②已知:20℃时硫酸钠的溶解度为19.5g。若要将反应后所得溶液恰好转化为20℃时的饱和溶液,最简单的方法是_____。
【答案】橡皮 90mL 4 加入硫酸到10mL一直是升高温度,而第4组实验竟然比第3组实验温度低 4.1% 加入硫酸钠至硫酸钠不再溶解
【解析】
根据给出的数据分析数据的合理性;消耗的硫酸的质量和对应的化学方程式求算所得溶液中溶质的质量分数。
(1)①首先,该小组同学将配制好的10%的氢氧化钠溶液,由于氢氧化钠和玻璃能反应,所以盛放氢氧化钠溶液的细口瓶应该使用橡皮塞。所以配置好的氢氧化钠溶液倒入带 橡皮塞的细口瓶中,备用。 用如表标签所示的浓硫酸配制100g溶质质量分数为9.8%的稀硫酸。所需水的质量为100g﹣![]() =90g折合90mL。故填:橡皮;90mL
=90g折合90mL。故填:橡皮;90mL
②其中实验组别为4数据明显不合理,判断理由是加入硫酸到10mL一直是升高温度,而第4组实验竟然比第3组实验温度低。故填:4;加入硫酸到10mL一直是升高温度,而第4组实验竟然比第3组实验温度低
(2)他们取稀释后的氢氧化钠溶液25g,向其中加入溶质质量分数为9.8%的稀硫酸,pH=7为恰好完全反应,消耗的稀硫酸的质量为10g,所以消耗的硫酸的质量为10g×9.8%=0.98g,所得溶液为25g+10g=35g。设所得溶液中溶质的质量分数为x。
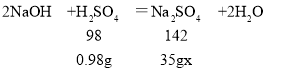
![]()
x≈4.1%
20℃时硫酸钠的溶解度为19.5g。若要将反应后所得溶液恰好转化为20℃时的饱和溶液,最简单的方法是加入硫酸钠至硫酸钠不再溶解。故填:4.1%;加入硫酸钠至硫酸钠不再溶解

【题目】某班学生在老师指导下探究铁与水蒸气的反应。
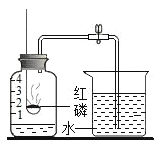
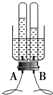
(1)按图甲装好药品,连接装置(夹持仪器已略去)。其中A装置的作用是________。
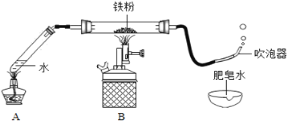
(2)加热一段时间后,灰色铁粉逐渐变黑,吹泡器连续吹出气泡,且气泡向上飞起;用燃着的木条靠近气泡,能产生爆鸣。该气体燃烧的化学方程式为_____________。
(3)同学们讨论后认为:铁与水蒸气反应生成的固体是“铁的一种氧化物”,玻璃管内的黑色固体中还可能含有“过量的铁”。
(查阅资料)铁有三种氧化物(FeO、Fe2O3、Fe3O4),其中FeO接触到空气会立即由黑色变为红棕色;铁的三种氧化物都不与硫酸铜溶液反应。
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
倒出玻璃管中黑色固体,平铺于白纸上 | 黑色固体不变色 | 黑色固体中一定没有____(填物质名称) |
取上述黑色固体少许,装入试管,加入足量____溶液 | ________,且有红色固体出现 | 黑色固体中一定含有__________ |
(探究结论)铁与水蒸气发生置换反应,有关的化学方程式是________________________。