题目内容
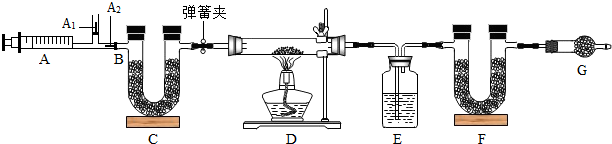
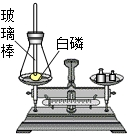 如图是测定白磷燃烧前后质量的变化情况,用来检验质量守恒的实验,试回答:
如图是测定白磷燃烧前后质量的变化情况,用来检验质量守恒的实验,试回答:①此反应是否符合质量守恒定律?
②白磷燃烧时,观察到的现象是
③做这个实验前锥形瓶应预先装少量的细砂的原因是
④将橡皮塞上的玻璃棒放在酒精灯上灼烧到红热后,迅速用橡皮塞将锥形瓶塞紧,并将白磷引燃,这里要“迅速用橡皮塞将锥形瓶塞紧”的原因是
⑤若上述的橡皮塞没有塞紧,结果天平的指针将会
⑥在上述的实验中有时会出现:白磷燃烧后,瓶塞突然“冲出”瓶口,如何改进装置避免这种现象?改进:
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和;
化学反应前后,元素的种类不变,原子的种类、总个数不变.
化学反应前后,元素的种类不变,原子的种类、总个数不变.
解答:解:①化学反应都遵循质量守恒定律;
因为反应前后原子种类不变,原子数目不变,原子质量不变,所以遵循质量守恒定律.
故填:符合;原子种类;原子数目;原子质量.
②白磷燃烧时,观察到的现象是产生大量白烟.
故填:产生白烟.
③做这个实验前锥形瓶应预先装少量的细砂的原因是防止锥形瓶受热炸裂.
故填:防止锥形瓶受热炸裂.
④要“迅速用橡皮塞将锥形瓶塞紧”的原因是防止空气和生成物逸散到空气中.
故填:防止空气和生成物逸散到空气中.
⑤若上述的橡皮塞没有塞紧,生成的五氧化二磷有一部分会逸散到空气中,结果天平的指针将会向右偏.
故填:b.
⑥改进方法可以是:在锥形瓶口插一根导管,上端口系一气球.
故填:在锥形瓶口插一根导管,上端口系一气球.
因为反应前后原子种类不变,原子数目不变,原子质量不变,所以遵循质量守恒定律.
故填:符合;原子种类;原子数目;原子质量.
②白磷燃烧时,观察到的现象是产生大量白烟.
故填:产生白烟.
③做这个实验前锥形瓶应预先装少量的细砂的原因是防止锥形瓶受热炸裂.
故填:防止锥形瓶受热炸裂.
④要“迅速用橡皮塞将锥形瓶塞紧”的原因是防止空气和生成物逸散到空气中.
故填:防止空气和生成物逸散到空气中.
⑤若上述的橡皮塞没有塞紧,生成的五氧化二磷有一部分会逸散到空气中,结果天平的指针将会向右偏.
故填:b.
⑥改进方法可以是:在锥形瓶口插一根导管,上端口系一气球.
故填:在锥形瓶口插一根导管,上端口系一气球.
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案
相关题目
NH4Cl 70℃时的溶解度为60克,此温度下,把14克NH4Cl放入20克水中,充分搅拌溶解,所得溶液的质量是( )
| A、34克 | B、27.5克 |
| C、32克 | D、12.75克 |

 为确定某硫酸铜粉末中是否混有硫酸钠,该实验小组同学先用托盘天平称取50g该粉末,溶于水配成219.6g溶液,再往其中加入溶质质量分数为8%的NaOH溶液,发生如下反应:
为确定某硫酸铜粉末中是否混有硫酸钠,该实验小组同学先用托盘天平称取50g该粉末,溶于水配成219.6g溶液,再往其中加入溶质质量分数为8%的NaOH溶液,发生如下反应: