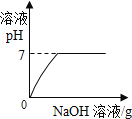
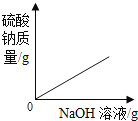
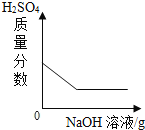
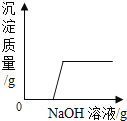
题目内容
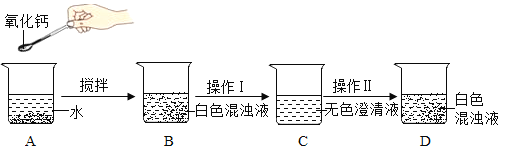
【题目】现有一固体混合物A,其中可能含铁、铜、碳酸钠三种物质中的两种或多种,还有一固体混合物B,其中可能含硝酸铵、氯化镁、硫酸铜三种物质中的两种或多种。按图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全进行)。
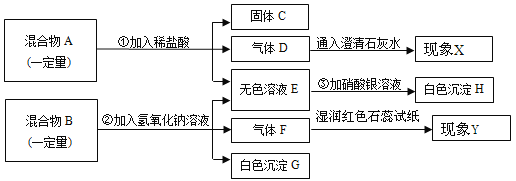
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)固体C的成分为(写化学式)________;现象Y为____________________。
(2)溶液E中肯定存在的酸根离子是__________(写离子符号)。
(3)在混合物A中,一定不存在的物质是________(写化学式)。
(4)写出过程③中发生的反应的化学方程式____________________。
(5)在混合物B中,上述三种物质中肯定存在的物质是______________(写化学式)。请简述其中一种物质存在的理由____________________。
【答案】Cu 红色石蕊试纸变蓝 ![]() 、
、![]() Fe NaCl+AgNO3=AgCl↓+NaNO3 NH4NO3、MgCl2 混合物B中加入氢氧化钠溶液产生气体,三种物质中能与碱反应生成气体的只有NH4NO3
Fe NaCl+AgNO3=AgCl↓+NaNO3 NH4NO3、MgCl2 混合物B中加入氢氧化钠溶液产生气体,三种物质中能与碱反应生成气体的只有NH4NO3
【解析】
碳酸钠和盐酸反应生成的二氧化碳,二氧化碳能使澄清石灰水变浑浊,铁和盐酸反应生成浅绿色的氯化亚铁,铜不会与酸反应;硝酸铵和碱反应生成的氨气能使石蕊变蓝色,镁离子和氢氧根离子会生成白色的氢氧化镁沉淀,铜离子和氢氧根离子生成蓝色的氢氧化铜沉淀.
(1)通过推导可知,固体C的成分为铜(![]() ),气体F的名称为氨气能使红色石蕊试纸变蓝;
),气体F的名称为氨气能使红色石蕊试纸变蓝;
(2)硝酸铵和氢氧化钠反应生成氨气、硝酸钠、水,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,镁离子和氢氧根离子会生成白色的氢氧化镁沉淀,所以溶液E中肯定存在的酸根离子是氯离子(![]() )、硝酸根离子(
)、硝酸根离子(![]() );
);
(3)通过推导可知,在混合物A里,一定不存在的物质是铁(![]() );
);
(4)过程③中是氯化钠和硝酸银反应产生氯化银沉淀和硝酸钠,反应的方程式为:![]() ;
;
(5)通过推导可知,在混合物B里,上述三种物质当中肯定存在的物质是![]() ,其中一种物质存在的理由是:混合物B中加入氢氧化钠溶液产生气体,三种物质中能与碱反应生成气体的为
,其中一种物质存在的理由是:混合物B中加入氢氧化钠溶液产生气体,三种物质中能与碱反应生成气体的为![]() 。
。

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案【题目】铁、铝、铜是常见的三种金属.同学们发现生活中的铝和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理.
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格.
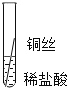
将粗细相同的铁丝、铝丝、铜丝分别插人体积相同、溶质质量分数也相同的稀盐酸中:
操作 |
|
|
| 根据现象得出金属活动性顺序 |
片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 | Fe>Al,Fe>Cu |
几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 |
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面致密的氧化膜会先与盐酸反应.
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是 .
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
操作 |
|
| 根据现象得出金属活动性顺序 |
现象 | 无明显现象 | 铁丝表面有红色物质析出 | Al>Fe>Cu |
写出铁与硫酸铜溶液反应的化学方程式 .
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插人顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序.金属丝的插入顺序为 .
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序 .