题目内容
【题目】在一定条件下,氨气与氧化铜反应生成红色固体、水及一种气体单质。某兴趣小组用如下装置探究该反应。已知氧化亚铜(Cu2O)为红色固体,能与稀硫酸反应:Cu2O+H2SO4=CuSO4+Cu+H2O。

(1)A处可用加热浓氢氧化钠溶液和硫酸铵的混合物制取氨气,反应方程式为 ,A处发生装置是 (选填右图装置编号),右图发生装置乙中仪器X的名称是 。

(2)装置D和装置 组合证明有水生成,装置E中应盛有的试剂是 。
(3)装置F为排水法收集气体,这是利用了气体的 ,实验时应等 时开始收集气体,进一步实验检验出该气体。
(4)充分反应后,取装置C中红色固体少许,加入适量稀硫酸,观察到 现象,说明固体物质为单质铜,装置C中反应的化学方程式是 。
【答案】(1)化学反应方程式略, 丙, 烧瓶。(2)B, 浓硫酸。
(3)气体难溶于水; 导管口产生连续均匀地气泡。
(4)液体没有变成蓝色, 化学反应方程式略
【解析】
试题分析∶这是一道实验探究题,(1)根据质量守恒定律,可写出化学方程式。液固加热制取气体可用丙。(2)碱石灰吸收二氧化碳,无水硫酸铜遇水变蓝。(3)气体难容于水,可用排水法。产气稳定在收集,标志连续均匀地冒气泡。⑷铜与硫酸不反应。
考点∶考查实验探究的基本思路和方法。

 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案【题目】我国青海湖采集的天然碱样品可表示为aNa2CO3·bNaHCO3·cH2O(a、b、c为最简整数比)。小红同学为测定其组成,称取该天然碱样品16.6g进行如下实验:
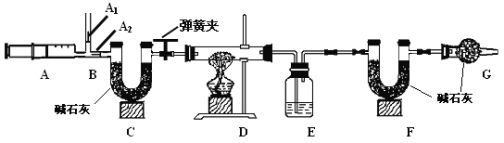
已知:1.碳酸钠比较稳定,加热不分解;
2. 2NaHCO3![]() Na2CO3 +CO2 ↑+H2O
Na2CO3 +CO2 ↑+H2O
3.图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,
A1打开进空气,A2关闭。
(一)实验步骤
(1)实验时,组装好装置,实验前应先 ,后续实验步骤是:
① 反复推拉注射器
② 称量E、F的质量
③ 关闭弹簧夹,加热D处试管直到反应不再进行
④ 打开弹簧夹,再次反复缓缓推拉注射器
⑤ 再次称量E、F的质量。
(二)问题探究:
(2) E中的药品为 ,E的作用是 。实验过程中,C的作用是 , F的作用是 。写出 F装置中所发生反应的一个化学方程式 。
(3)实验步骤②与③能否颠倒 (填“能”或“不能”)。若不进行步④的操作,则所测得的碳酸氢钠质量 (填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是 ;若没有G装置,则碳酸氢钠的质量 (填“偏大”、“偏小”、“无影响”)。
(4)下表是实验记录数据:
反应前 | 反应后 |
E的质量为100.0g | E的质量为102.25g |
F的质量为50.0g | F的质量为51.1g |
则: ① 碳酸氢钠分解生成二氧化碳的质量为 g
② 碳酸氢钠的质量为 g
③ 该天然碱的化学式中a:b:c= 。
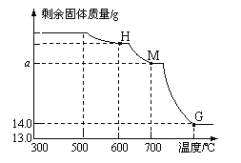
【题目】铁的锈浊对社会生产造成较大损害,但也有有利的一面,如某些食品包装袋内常放入还原性铁粉作“双吸剂”以防止食品腐败.某课外兴趣小组在实验室发现了一包破损的还原性铁粉(含少量杂质,杂质既不溶于水也不溶于酸),他们取六份样品,分别加稀硫酸反应.测得部分数据加下,请根据有关信息冋答问题.
实验次数 | 1 | 3 | 4 | 5 | 6 |
取样品质量(g) | 31.0 | 31.0 | 31.0 | 31.0 | 31.0 |
取稀硫酸质量(g) | 30.0 | 90.0 | 120.0 | 150.0 | 180.0 |
产生气体质量(g) | 0 | a | 0.3 | 0.5 | 0.6 |
(1)食品袋内放入“双吸剂”是为了吸收 ,用铁粉而不用铁块作“双吸剂”的理由是 .
(2)a的数值为 .
(3)第4次实验,所得到溶液中溶质的化学式为 .
(4)列式计算该样品中单质铁的质量分数(保留至0.1%).